【答案】
分析:(1)加入药品时,为防止酸液飞溅,应先加入乙醇再加入浓硫酸和乙酸;酯化反应的本质为酸脱羟基,醇脱氢;
(2)根据粗产品乙酸乙酯、乙酸和乙醇的混合物中各自的性质,进行解答;
(3)乙酸与乙醇需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动;
(4)用饱和碳酸钠溶液吸收乙酸乙酯,乙醇溶解,碳酸钠与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度;
(5)根据实验操作和实验现象进行解答;
解答:解:(1)浓硫酸溶于水放出大量的热,加入药品时,为防止酸液飞溅,应先加入乙醇再加入浓硫酸和乙酸,如先加浓硫酸会出现酸液飞溅的可能现象;实验中用乙醇与乙酸作用,酯化反应的本质为酸脱羟基,醇脱氢,该反应生成乙酸乙酯和水,且为可逆反应,所以乙酸脱羟基,乙醇脱氢离子,
故答案为:向试管倒入一定量的乙醇,然后边摇动试管边慢慢加入一定量的浓硫酸和一定量的醋酸;CH
3COOH+CH
3CH
2OH

CH
3COOC
2H
5+H
2O;
(2)乙酸乙酯中混有乙醇和乙酸,二者易溶于水而产生倒吸,故答案为:防止倒吸;
(3)乙酸与乙醇需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动.故浓硫酸的作用为催化剂,吸水剂,故答案为:催化作用;吸水作用;
(4)制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,目的是除去乙醇和乙酸、降低乙酸乙酯的溶解度,便于分层.
故答案为:除去乙醇和乙酸、降低乙酸乙酯的溶解度,便于分层;
(5)在碳酸钠溶液层上方有无色油状液体出现,闻到香味,说明实验中生成的乙酸乙酯,其密度比水小;分离粗产品乙酸乙酯、乙酸和乙醇的混合物,加入饱和碳酸钠溶液,实现酯与乙酸和乙醇的分离,分离油层和水层采用分液的方法即可,所以用到的仪器为分液漏斗,故答案为:小;分液漏斗;
点评:本题考查了乙酸乙酯的制备,注意把握乙酸乙酯的制备原理和实验方法,把握乙酸乙酯与乙酸、乙醇性质的区别,题目难度不大.

 CH3COOC2H5+H2O;
CH3COOC2H5+H2O;

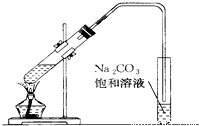
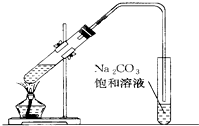 如图是实验室制取乙酸乙酯的装置.
如图是实验室制取乙酸乙酯的装置. 如图是实验室制乙酸乙酯的装置.
如图是实验室制乙酸乙酯的装置.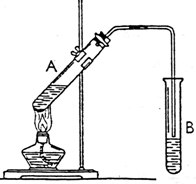 如图为实验室制取乙酸乙酯的装置图.试回答:
如图为实验室制取乙酸乙酯的装置图.试回答: