
| A. | 1 mol S与足量Fe反应,转移的电子数为3NA个 | |
| B. | 1.5 mol NO2与足量H2O反应,转移的电子数为2NA个 | |
| C. | 常温常压下,46 g的NO2和N2O4混合气体含有的原子数为3NA个 | |
| D. | 100 ml 0.10mol/L的氨水中,含NH3•H2O 分子0.01NA个 |
分析 A、氯气和铁反应生成氯化铁,电子转移按照全部反应的氯气计算;
B、二氧化氮和水的反应中,二氧化氮既是氧化剂又是还原剂;
C、NO2和N2O4具有相同的最简式NO2;
D、n=CV,一水合氨是弱电解质存在电离平衡.
解答 解:A、氯气和铁反应生成氯化铁,电子转移按照全部反应的氯气计算,转移电子2NA,故A错误;
B、二氧化氮和水的反应3NO2+H2O═2HNO3+NO,1.5molNO2与足量H2O反应,转移的电子数以生成的NO计算为0.5×2NA=NA,故B错误;
C、NO2和N2O4具有相同的最简式NO2,46g的NO2和N2O4混合气体含有的原子数为$\frac{46g}{46g/mol}$×3NA=3NA,故C正确;
D、100 ml 0.10mol/L的氨水中,溶质物质的量=0.1L×0.1mol/L=0.01mol,一水合氨是弱电解质存在电离平衡,含NH3•H2O 分子小于0.01NA个,故D错误;
故选C.
点评 本题考查学生有关阿伏伽德罗常熟的有关计算知识,主要是气体摩尔体积条件分析,氧化还原反应电子转移计算,物质的量和微粒数的计算分析,可以根据所学知识来回答,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 可能等于7 | B. | 一定<7 | C. | 一定>7 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
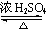 CH3COOCH2CH=CH2+H218O,酯化反应生成的产物在一定条件下可以发生加聚反应得到高分子化合物,其结构简式
CH3COOCH2CH=CH2+H218O,酯化反应生成的产物在一定条件下可以发生加聚反应得到高分子化合物,其结构简式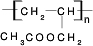 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
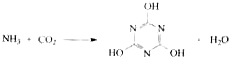 下列有关三聚氰胺的说法正确的是( )
下列有关三聚氰胺的说法正确的是( )| A. | 分子式为C3H6N3O3 | B. | 分子中既含极性键,又含非极性键 | ||
| C. | 属于共价化合物 | D. | 生成该物质的上述反应为中和反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⑥>⑤>④>①>③>② | B. | ⑥>④>⑤>①>③>② | C. | ⑥>④>⑤>①>②>③ | D. | ⑥>⑤>④>①>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
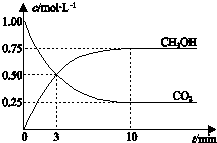
| A. | 升高温度能使$\frac{c(C{H}_{3}OH)}{c(C{O}_{2})}$ 增大 | |
| B. | 反应达到平衡状态时,CO2的平衡转化率为75% | |
| C. | 3 min时,用CO2的浓度表示的正反应速率等于用CH3OH的浓度表示的逆反应速率 | |
| D. | 从反应开始到平衡,H2的平均反应速率υ(H2)=0.075 mol•L-1•min-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com