
科目:高中化学 来源:2015-2016学年重庆市高二下第四次月考化学试卷(解析版) 题型:选择题
4.6g铜镁合金完全溶解于100mL密度为1.40g/mL、质量分数为63%的浓硫酸中,得到4480mLNO2和336mLN2O4的混合气体(标准状况),向反应后的溶液中加入1.0mol•L-1NaOH溶液至离子恰好全部沉淀时,下列说法不正确的是
A.该合金中铜与镁的物质的量之比是46:69
B.该浓硝酸中HNO3的物质的量浓度是14.0mol/L
C.产生沉淀8.51g
D.离子恰好完全沉淀时,加入NaOH溶液的体积是230mL
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆一中高二下学期期中化学试卷(解析版) 题型:选择题
一定温度下,W g下列物质在足量氧气中充分燃烧,产物与过量的Na2O2完全反应,Na2O2固体增重W g,符合此要求的组合是:
① H2 ② CO ③ CO和H2 ④ HCOOCH3 ⑤ OHC-CHO
A.除⑤外 B.仅④⑤ C.仅①②③ D.全部
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州凯里一中高一下期中理科化学试卷(解析版) 题型:填空题
A、B、C、D 4种元素的核电荷数依次增大,它们的离子的电子层数相同且最外层电子数均为8。A原子的L层 电子数与K、M层电子数之和相等,D原子的K、L层电子数之和等于电子总数的一半。
电子数与K、M层电子数之和相等,D原子的K、L层电子数之和等于电子总数的一半。
请回答下列 问题:
问题:
(1)4种元素的符号依次是A________,B_________, C_________,D________。它们原子的半径由大到小的顺序是(要求写出化学符号)______________________________ ___。
___。
(2)C和D元素对应的最高 价氧化物对应水化物的碱性强弱顺序(要求写出化学式)__________。
价氧化物对应水化物的碱性强弱顺序(要求写出化学式)__________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州凯里一中高一下期中理科化学试卷(解析版) 题型:选择题
下列各组材料中不能组成原电池的是( )
A.锌片、石墨、硫酸溶液 B.铜片、银片、氯化铁溶液
C.锌片、铜片、乙醇溶液 D.铁片、铜片、稀盐酸
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州凯里一中高一下期中理科化学试卷(解析版) 题型:选择题
根据元素周期表和元素周期律分析下面的推断,其中错误的是( )
A.铍(Be)的原子失电子能力比镁弱
B.砹(At)的氢化物不稳定
C.硒(Se)化氢比硫化氢稳定
D.氢氧化锶[Sr(OH)2]比氢氧化钙的碱性强
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二5月月考理科化学试卷(解析版) 题型:实验题
(I)有机物M(分子式:C6H4S4)是隐形飞机上吸波材料的主要成分。某化学兴趣小组为验证其组成元素,进行了如下实验:将少量样品放入A的燃烧管中,通入足量O2,用电炉加热使其充分燃烧,并将燃烧产物依次通入余下装置。(右图中的夹持仪器的装置已略去) 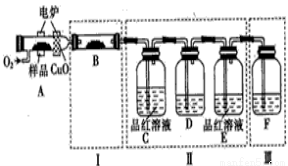
(1)装置B的目的是验证有机物中含氢元素,则B中盛装的试剂名称为 ________;
(2)能证明有机物含碳元素的现象是__________;
(3)指出装置F中的错误: ________。
(II)苯甲酸的重结晶实验基本操作如下:①将粗苯甲酸1g加到100mL的烧杯中,再加入50mL蒸馏水,在石棉网上边搅拌边加热,使粗苯甲酸溶解,②全溶后再加入少量蒸馏水并搅拌.③然后,使用短颈玻璃漏斗趁热将溶液过滤到另一100mL烧杯中,将滤液静置,使其缓慢冷却结晶.④滤出晶体。
回答下列问题:
(1)上述四步操作过程中需用到玻璃棒的步骤有____________;
(2)步骤②的目的是____________________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二5月月考理科化学试卷(解析版) 题型:选择题
警察常从案发现场的人体气味来获取有用线索,人体气味的成分中含有以下化合物:①辛酸;②壬酸;③环十二醇;④5,9一十一烷酸内酯;⑤十八烷;⑥己醛;⑦庚醛。下列说法正确的是( )
A.①、②、⑥分子中碳原子数小于10,③、④、⑤、⑦分子中碳原子数大于10
B.①、②是无机物,③、⑤、⑦是有机物
C.①、②是酸性化合物,③、⑤不是酸性化合物
D.②、③、④含氧元素,⑤、⑥、⑦不含氧元素
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海师大附二中高一下期中化学试卷(解析版) 题型:填空题
有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入6mol/LH2SO4溶液中,乙同学将电极放入6mol/LNaOH溶液中,如图:
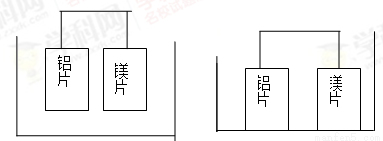
甲(H2SO4溶液) 乙(NaOH溶液)
(1)写出甲池中正极的电极反应式: ,负极的电极反应式: 。
(2)写出乙池中负极的电极反应式: ,乙池中总反应的离子方程式: 。
(3)如果甲和乙同学均认为,“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出 活动性更强,而乙会判断出 活动性更强。
(5)丙同学依据甲、乙同学的思路,设计如下实验:将铝片和铜片用导线相连.一组插入浓硝酸中,一组插入稀NaOH溶液中,分别形成了原电池。
①在这两个原电池中,负极分别为________。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片 D.铜片、铜片
②写出插入浓硝酸中形成原电池的总反应化学方程式__________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com