
| A. | Al(OH)3分解的产物可用于制备金属铝 | |
| B. | 电解熔融氯化钠所得到的金属钠呈液态 | |
| C. | MgO的熔点很高,可用于制作耐高温材料 | |
| D. | 电解MgCl2水溶液,可制得金属镁 |
分析 A、工业上电解氧化铝制取Al;
B、Na熔点很低;
C、根据MgO的物理性质来分析其应用;
D、根据电解氯化镁溶液的反应原理及其产物来判断.
解答 解:A、Al(OH)3分解生成氧化铝,工业上电解氧化铝制取Al,故A正确;
B、NaCl熔点很高,Na熔点很低,电解熔融的NaCl制取的Na为液态,故B正确;
C、MgO的熔点很高,可用于制作耐高温材料,故C正确;
D、电解MgCl2饱和溶液,发生的化学反应为:MgCl2+2H2O$\frac{\underline{\;通电\;}}{\;}$Mg(OH)2↓+H2↑+Cl2↑,不会产生金属镁,电解熔融的MgCl2能制取单质镁,发生的反应MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑,故D错误;
故选D.
点评 本题考查了金属的冶炼、Mg及其化合物的性质,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 氯化氢分子的电子式: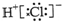 | B. | 乙烯的分子式:C2H6 | ||
| C. | 二氧化碳分子的结构式:O-C-O | D. | CH4分子的球棍模型: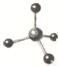 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 项目 | 物质 | 杂质(少量) | 试剂 | 操作方法 |
| A | CO2 | SO2 | 饱和NaHCO3溶液 | 洗气 |
| B | 硝酸 | 盐酸 | 过量的AgNO3溶液 | 过滤 |
| C | 溴苯 | 溴 | 加入CCl4 | 分液 |
| D | Na2CO3 | Na2SO4 | 加入适量BaCl2溶液 | 溶解、过滤、洗涤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2是酸性氧化物,但不能直接与水反应生成H2SiO3 | |
| B. | 常温下浓硝酸与铝不反应,可用铝制容器存放浓硝酸 | |
| C. | 氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 | |
| D. | Na2O2能与CO2反应产生O2,可用作呼吸面具的供氧剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
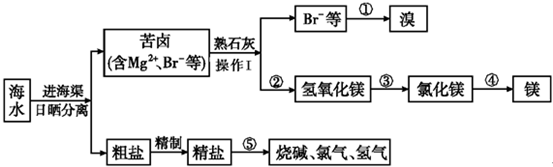
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制取水泥和玻璃的原料中都含有石灰石 | |
| B. | 普通玻璃是电的绝缘体,这种透明的固体物质属于晶体 | |
| C. | 石英玻璃能经受温度剧变且抵抗酸碱的腐蚀 | |
| D. | 硅酸盐可用氧化物表示其组成,这表明硅酸盐是由氧化物组成的 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 +H+=
+H+=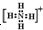 ;由5个原子核10个电子组成的化合物电子式是
;由5个原子核10个电子组成的化合物电子式是 ,结构式是
,结构式是 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com