
| A.未将烧杯和玻璃棒的洗涤液移入容量瓶 |
| B.溶解搅拌时液体飞溅 |
| C.定容时俯视容量瓶瓶颈刻度线 |
| D.摇匀后见液面下降,再加水至刻度线 |
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中 |
| B.配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 |
| C.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D.从碘水中提取单质碘时,可以用无水乙醇代替CCl4 |
| E.配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
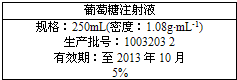
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 实验步骤 | 有关问题 |
| (1)计算所需KCl的质量 | 需要KCl的质量为______g |
| (2)称量KCl固体 | 称量过程中主要用到的仪器是: ______ |
| (3)将KCl加入100mL烧杯中,并加入适量水 | 为了加快溶解速率,可以采取哪些措施: ______ |
| (4)将烧杯中溶液转移至500mL容量瓶中 | 为了防止溶液溅出,应采取什么措施: ______ |
| (5)向容量瓶中加蒸馏水至刻度线 | 在进行此操作时应注意什么问题: ______ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将胆矾加热除去结晶水后,称取16g溶解在1L水当中 |
| B.称取胆矾25g,溶解在1L水当中 |
| C.将25g胆矾溶于水,然后将此溶液稀释至1L |
| D.将16g胆矾溶于水,然后将此溶液稀释至1L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com