
 实验室在蒸馏烧瓶中加NaBr、适量水、95%的乙醇和浓硫酸,边反应边蒸馏,蒸出的溴乙烷用水下收集法获得.反应的化学方程式为:
实验室在蒸馏烧瓶中加NaBr、适量水、95%的乙醇和浓硫酸,边反应边蒸馏,蒸出的溴乙烷用水下收集法获得.反应的化学方程式为:| △ |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
其中可能发生的副反应有:2HBr+H2SO4(浓)=====Br2+SO2↑+2H2O,已知CH3CH2Br的沸点为38.4℃,密度比水大,为常温下不溶于水的油状液体。
请回答下列问题:
(1)反应中加入适量的水,除为了溶解NaBr外,作用还有:①________;②________。
(2)为了保证容器均匀受热和控制恒温,加热方法最好采用________。
(3)烧瓶中的导气管在瓶塞上的垂直部分比其他同种装置中的导管要长些的原因是________。
(4)本实验是否需要采用边反应边蒸馏的操作设计?
(5)溴乙烷可用水下收集法获得的依据和从水中分离的方法是________。
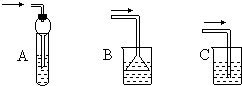
(6)下列装置在实验中既能吸收气体,又能防止液体倒吸的是________(填标号)。

查看答案和解析>>
科目:高中化学 来源: 题型:058
实验室在蒸馏烧瓶中加NaBr、适量水、95%的乙醇和浓H2SO4,边反应边蒸馏,蒸出的溴乙烷用水下收集法获得。反应式为:![]()
![]()
其中可能发生的副反应有:2HBr+H2SO4(浓)=====Br2+SO2↑+2H2O,已知CH3CH2Br的沸点为38.4℃,密度比水大,为常温下不溶于水的油状液体。
请回答下列问题:
(1)反应中加入适量的水,除为了溶解NaBr外,作用还有:①________;②________。
(2)为了保证容器均匀受热和控制恒温,加热方法最好采用________。
(3)烧瓶中的导气管在瓶塞上的垂直部分比其他同种装置中的导管要长些的原因是________。
(4)本实验是否需要采用边反应边蒸馏的操作设计?
(5)溴乙烷可用水下收集法获得的依据和从水中分离的方法是________。
(6)下列装置在实验中既能吸收气体,又能防止液体倒吸的是________(填标号)。

查看答案和解析>>
科目:高中化学 来源:同步题 题型:实验题
 C2H5Br+H2O
C2H5Br+H2O 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com