
����Ŀ������˵�����ж���ȷ���ǣ� ��
A.����ϵͳ����Ϊ1������2���һ�����������������ʽΪC11H24
B.��ȩ�ͱ�ϩȩ��CH2=CHCHO������ͬϵ�������������ַ�Ӧ��IJ���Ҳ����ͬϵ��
C.ͨ���ⶨ��Ӧǰ����Һ�����Եı仯���ж���ϡ������Һ�м�������Ũ��ˮʱ��������ȡ����Ӧ�����Ǽӳɷ�Ӧ
D.ú���ӹ����õIJ����д��ڴ����Ķ�����ͳ�������������������� ![]() ��������
�������� ![]() �����죨
�����죨 ![]() ���ȣ���Щ���������ڱ���ͬϵ��
���ȣ���Щ���������ڱ���ͬϵ��
���𰸡�C
���������⣺A�����������в��ܳ���1������2���һ�������˵��ѡȡ�����������̼������1������2���һ��������������������A����B����ȩ�ͱ�ϩȩ�� ![]() ���Ľṹ��ͬ�����Զ���һ������ͬϵ�������������ַ�Ӧ��ֱ������Ҵ��ͱ����������������ӳɵIJ�������ͬϵ���B����
���Ľṹ��ͬ�����Զ���һ������ͬϵ�������������ַ�Ӧ��ֱ������Ҵ��ͱ����������������ӳɵIJ�������ͬϵ���B����
C�����������������ӳɷ�Ӧ����Ӧ����Һ�����Ա仯���䣬��Ϊȡ����Ӧ����Ӧ����Һ��������ǿ����ͨ���ⶨ��Ӧǰ����Һ�����Եı仯���ж���ϡ������Һ�м�������Ũ��ˮʱ��������ȡ����Ӧ�����Ǽӳɷ�Ӧ����C��ȷ��
D������������ ![]() ��������
�������� ![]() �����죨
�����죨 ![]() �������ϱ���ͬϵ���ͨʽCnH2n��6 �� ���DZ���ͬϵ���D����
�������ϱ���ͬϵ���ͨʽCnH2n��6 �� ���DZ���ͬϵ���D����
��ѡC��
�����㾫����������Ĺؼ��������ⷼ������������ͬϵ������֪ʶ�����շ����ﺬ��һ������������̼�⻯�����Ϊ��������������һ�������ͱ���������ɵķ������б���ͬϵ���ͨʽΪCnH2n�C6��n��6����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ������������ȷ����(����)
A. ���ʵ���Ũ��Ϊ0.5 mol/L��MgCl2��Һ�У�����Cl������ĿΪ NA
B. 11.2 g Fe������ˮ������Ӧ�����ɵ�H2������ĿΪ0.3 NA
C. ��״���£�22.4LH2O���еķ�����ΪNA
D. 2.3 g Na��һ����������Ӧ����Na2O��Na2O2�Ļ���ת�Ƶĵ�����һ��Ϊ0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��400 mLijŨ�ȵ�NaOH��Һ��5.6 L Cl2����״����ǡ����ȫ��Ӧ�����㣨д����Ҫ�ļ�����̣���
��1�����ɵ�NaClO�����ʵ�����_____________
��2������Һ��NaOH�����ʵ���Ũ�ȡ�__________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1989������������֯����ȷ��ΪʳƷ��ȾԴ֮һ�����Կ���ʹ�á���������Ӧ��ʱӦ���Կ��Ƶ���
�������Ͻ� ���Ƶ��� ���ƴ��� ��������ˮ ���������մ���ʳƷ���ɼ�
�������������������ӹ���θ��ƽҩƬ �������� ���װ�ǹ���СʳƷ
A. �ۢݢߢ� B. �ޢߢ� C. �ۢݢ� D. �ۢܢݢޢߢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�������ƽ��������Ϊ126���춬������R��Ϊ����C2H4ON�������з���ʽΪCXHYOZN17S2��һ����������������2���춬����������ɡ���ö��ĵķ��������ԼΪ
A. 1638B. 1854C. 1890D. 2142
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����������ʺ���;��˵����ȷ���ǣ� ��
A.þ���������ȶ��Ҷ��к�ǿ�Ŀ���ʴ����������þ���Ͻ�����ڷɻ����ִ�����
B.Na2SiO3��Һ���������コ��ľ�ķ���������������Ʊ��轺��ԭ��
C.����������̼���ƾ�����������θ�����
D.ȱ����ƶѪ�ɷ�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ����ͨ��ʵ�鷽����֤Fe2+�����ʣ�
��1����ͬѧ��ʵ��ǰ������Fe2+���ԣ���д���±���
ʵ����� | Ԥ������ | ��Ӧ�����ӷ���ʽ |
��ʢ������FeSO4��Һ���Թ��е�������Ũ���ᣬ�� | �Թ��в�������ɫ���壬��Һ��ɫ��� | Fe2++NO |
���ձ��в�������ͬѧ����ʵ�飮�۲쵽Һ���Ϸ�������Ϊ����ɫ�����Թ�����Һ��ɫȴ��Ϊ����ɫ��
��2��Ϊ�˽�һ��̽����Һ�������ɫ��ԭ��ͬѧ��������ʵ�飮��ԭ����FeSO4��Һ�ͷ�Ӧ����Һ�о�����KSCN��Һ��ǰ�߲����ɫ�����ߣ���������Ũ�����FeSO4��Һ����죮������Ľ����� ��
��3����ͬѧͨ���������ϣ���Ϊ��Һ������ɫ������NO2��NO����Һ��Fe2+��Fe3+������Ӧ���õ��ģ�Ϊ����������ͼװ�ã��������Ѽ��飬β������װ���ԣ�����̽������������a���ر�b����ʹ��װ���з�Ӧ��ʼ�۲쵽������Һ��Ϊ����ɫ����������Һ�����Ա仯��
��������b���ر�a��һ��ʱ�����ֹͣ���з�Ӧ��
����Ϊ�뢡��ʵ����ж��գ����������������ʲ��䣩��ʹ���з�Ӧ�������۲쵽�������벽�袡����ͬ��
��ͭ������Ũ���ᷴӦ�Ļ�ѧ����ʽ����
��װ���ҵ���������
�۲��袢��Ŀ������
�ܸ�ʵ��ɵó��Ľ����� ��
��4����ͬѧ���½��У�1����ʵ�飬�۲쵽��Ԥ��������ʵ������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͪͨ������ɫҺ�壬��ˮ���ܣ��ܶ�С��1gmL��1���е�ԼΪ56�森Ҫ��ˮ���ͪ�Ļ�����н���ͪ�������������Ϊ���з�������Ϊ�������ǣ���������
A. ���� B. ��Һ C. ���� D. ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1��6�������ᣨG���Ǻϳ���������Ҫԭ��֮һ�����ú�����̼ԭ�ӵ��л������������Ʊ�����ͼΪAͨ��������Ӧ�Ʊ�G�ķ�Ӧ���̣����ܵķ�Ӧ�м�����ΪB��C��D��E��F���� 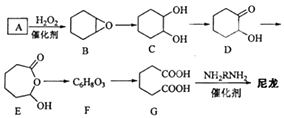
��1��������A�к�̼87.8%������Ϊ�⣬A�Ļ�ѧ����Ϊ ��
��2��C��D �ķ�Ӧ����Ϊ ��
��3��F�Ľṹ��ʽΪ ��
��4��B��C��D�����м������У��˴Ź������׳��������� �� ���ٵ��� ��
��5��������һ���л��߷��ӻ������G�ϳ������Ļ�ѧ����ʽΪ ��
��6����Aͨ��������Ӧ�Ʊ�1��3��������ϩ�ĺϳ�·��Ϊ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com