
【题目】已烯雌酚是一种激素类药物,结构如图,下列有关叙述中不正确的是( )
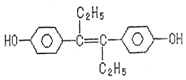
A.可与NaOH和![]() 发生反应
发生反应
B.可以用有机溶剂萃取
C.1mol该有机物可以与![]() 发生反应
发生反应
D.该有机物分子中,可能有18个碳原子共平面
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】25℃时0.1molNa2CO3与盐酸混合所得体积为1L的溶液中部分微粒与溶液pH值之间关系如图所示,下列叙述正确的是
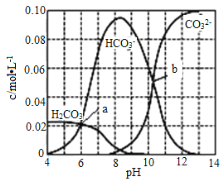
A.混合液随pH增大,![]() 先增大后减小
先增大后减小
B.b点时溶液中离子存在如下关系:2c(![]() )+c(
)+c(![]() )+c(OH-)=c(Na+)+c(H+)
)+c(OH-)=c(Na+)+c(H+)
C.H2CO3的一级电离常数Ka1约为10-6,Ka2的数量级为10-11
D.pH=7时,溶液中离子浓度大小顺序为:c(Na+)=c(Cl-)>c(![]() )>c(H+)=c(OH-)>c(
)>c(H+)=c(OH-)>c(![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为实验室制取少量乙酸乙酯的装置。下列关于该实验的叙述不正确的是( )
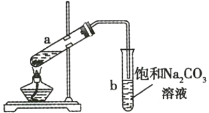
A.向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加入冰醋酸
B.试管b中导气管下端管口不能浸入液面下的原因是防止实验过程中发生倒吸
C.实验时加热试管a的目的之一是及时将乙酸乙酯蒸出,使平衡向生成乙酸乙酯的方向移动
D.试管b中饱和![]() 溶液的作用之一是吸收乙酸乙酯
溶液的作用之一是吸收乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.1mol某烃在氧气中充分燃烧,需要消耗氧气24.64L(标准状况下)。它在光照条件与氯气反应能生成四种一氯取代物。则该烃的结构简式可能是
A.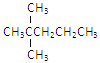
B.CH3CH2CH2CH2CH3
C.![]()
D.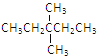
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于H2(g)+I2(g)![]() 2HI(g),ΔH<0,根据如图,下列说法错误的是( )
2HI(g),ΔH<0,根据如图,下列说法错误的是( )
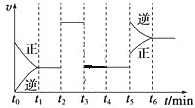
A.t2时可能使用了催化剂B.t3时可能采取减小反应体系压强的措施
C.t5时采取升温的措施D.反应在t6时刻,HI体积分数最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废旧电池材料的主要成分为钴酸锂(LiCoO2),还含有一定量的铁、铝、铜等元素的化合物,其回收工艺如图所示,最终可得到Co2O3和锂盐。
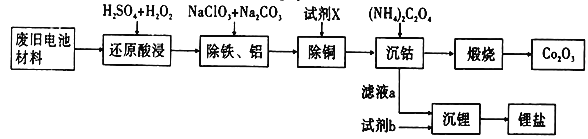
已知:CoC2O4·2H2O微溶于水,它的溶解度随温度升高而逐渐增大,且能与过量的C2O42-离子生成Co(C2O4)n2(n-1)-而溶解。
(1)“还原酸浸”过程中钴酸锂反应的离子方程式________________________________________;温度通常控制在40℃以下的原因是_______________________________________________。
(2)“除铝铁”过程的两种试剂的作用分别是____________________,______________________。
(3)“除铜”所用试剂X为H2S,试写出该反应的离子方程式______________________________。
(4)“沉钴”过程中,(NH4)2C2O4的加入量(图a)、沉淀反应的温度(图b)与钴的沉淀率关系如图所示:
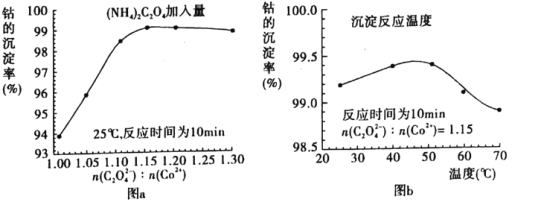
①随n(C2O42-):N(Co2+)比值的增加,钴的沉淀率先逐渐增大后又逐渐减小的原因________________________________________________________________________。
②沉淀反应时间为10 min,温度在50℃以上时,随温度升高而钴的沉淀率下降的可能原因是_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是甲、乙、丙、丁、戊五种有机物的有关信息:
甲 | ①能使溴的四氯化碳溶液退色;②比例模型为 |
乙 | ①由C、H两种元素组成;②球棍模型为 |
丙 | ①由C、H、O三种元素组成;②能与Na反应,但不能与 |
丁 | ①相对分子质量比丙少;②能由丙氧化而成 |
戊 | ①由C、H、O三种元素组成;②球棍模型为 |
回答下列问题:
(1)甲与溴的四氯化碳溶液反应所得产物的名称是___________________。
(2)甲与氢气发生加成反应后生成物质己,在己在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式![]() 。当
。当![]() ___________________时,这类有机物开始出现同分异构体。
___________________时,这类有机物开始出现同分异构体。
(3)乙具有的性质是___________________(填序号)。
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大 ⑤与酸性![]() 溶液和溴水反应而使其退色 ⑥任何条件下都不与氢气反应
溶液和溴水反应而使其退色 ⑥任何条件下都不与氢气反应
(4)丙与戊反应能生成相对分子质量为100的酯,所发生反应的反应类型为_____________________,对应的化学方程式为_______________________。
(5)写出丙氧化生成丁的化学反应方程式:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是( )
A. 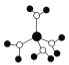 水合铜离子的模型如图所示,1个水合铜离子中有4个配位键
水合铜离子的模型如图所示,1个水合铜离子中有4个配位键
B. 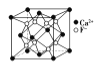 CaF2晶体的晶胞如图所示,每个CaF2晶胞平均占有4个Ca2+
CaF2晶体的晶胞如图所示,每个CaF2晶胞平均占有4个Ca2+
C.  H原子的电子云图如图所示,H原子核外的大多数电子在原子核附近运动
H原子的电子云图如图所示,H原子核外的大多数电子在原子核附近运动
D.  金属Cu中Cu原子堆积模型如图所示,该金属晶体为最密堆积,每个Cu原子的配位数均为12
金属Cu中Cu原子堆积模型如图所示,该金属晶体为最密堆积,每个Cu原子的配位数均为12
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com