
科目:高中化学 来源:不详 题型:单选题
| A.原子半径 A>B>D>C | B.原子序数?d>c>b>a |
| C.离子半径 C>D>B>A | D.单质的还原性 A>B>D>C |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 部分结构知识 | 部分性质 |
| X | X的单质由双原子分子构成,分子中有14个电子 | X有多种氧化物,如XO、XO2、X2O4等;通常情况下XO2与X2O4共存 |
| Y | Y原子的次外层电子数等于最外层电子数的一半 | Y能形成多种气态氢化物 |
| Z | Z原子的最外层电子数多于4 | Z元素的最高正化合价与最低负化 合价代数和等于6 合价代数和等于6 |
| W | W原子的最外层电子数等于2n-3(n为原子核外电子层数) | 化学反应中W原子易失去最外层电子形成Wn+ |
 。
。 性由强到弱的顺序是 。
性由强到弱的顺序是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 在同周期的主族元素中原子半径最大,W是地壳中含量最多的金属元素,L的单质晶体熔点高、硬度大,是一种重要的半导体材料。用化学用语回答下列问题:
在同周期的主族元素中原子半径最大,W是地壳中含量最多的金属元素,L的单质晶体熔点高、硬度大,是一种重要的半导体材料。用化学用语回答下列问题: 种新型无机非金属材料,其化学式是 。
种新型无机非金属材料,其化学式是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 间白色沉淀变为灰绿色,最终变为红褐色;
间白色沉淀变为灰绿色,最终变为红褐色;查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 学原理相
学原理相 同
同 s多4个
s多4个 质子
质子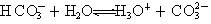
 的非金属性逐渐减弱,故氢卤酸的酸性依次减弱
的非金属性逐渐减弱,故氢卤酸的酸性依次减弱 2NH3
2NH3 (g) △H=-38.6kJ·mol-1
(g) △H=-38.6kJ·mol-1| A.全部 | B.④⑤ | C.②③④⑦ | D.②④⑦ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 天然气。
天然气。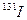 )是核裂变产物之一。
)是核裂变产物之一。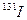 原子核内有53个质子,78个中子,关于
原子核内有53个质子,78个中子,关于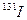 ,下列说法正确的是__________(填序号)。
,下列说法正确的是__________(填序号)。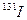 原子核外电子数为78 ②
原子核外电子数为78 ②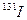 的相对原子质量约为131
的相对原子质量约为131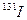 一旦被人体吸入会引发甲状腺疾病。服用含碘元素的物质可封闭甲状腺,让放射性碘无法“入侵”。我国规
一旦被人体吸入会引发甲状腺疾病。服用含碘元素的物质可封闭甲状腺,让放射性碘无法“入侵”。我国规 定在食盐中添加碘元素的标准为20-40mg/kg,若要达到防御
定在食盐中添加碘元素的标准为20-40mg/kg,若要达到防御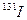 辐射的作用,一次需补充碘元素100mg。按每人每天食用10g加碘盐,则我们每天最多能从碘盐中吸收 ______ mg碘元素。
辐射的作用,一次需补充碘元素100mg。按每人每天食用10g加碘盐,则我们每天最多能从碘盐中吸收 ______ mg碘元素。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1s2 | B.3s23p1 | C.3s23p6 | D.4s2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com