
【题目】下面是关于蛋白质的论述,正确的是
A. 每种蛋白质都含有C、H、O、N、P、Fe元素
B. 每种蛋白质的分子结构中都含有肽键
C. 蛋白质都是酶
D. 蛋白质是调节细胞和生物体新陈代谢的唯一物质
科目:高中化学 来源: 题型:
【题目】下列事实能说明影响化学反应速率的决定性因素是反应物本身性质的是( )
A. Cu能与浓硝酸反应,而不与浓盐酸反应
B. 锌粉比锌粒与稀硫酸反应快
C. N2与O2在常温、常压下不反应,放电时可反应
D. Cu与浓硫酸能反应,而不与稀硫酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置适用于实验室制氨气并验证氨气的某化学性质,其中能达到实验目的的是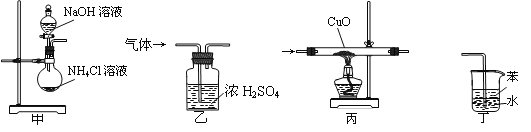
A.用装置甲制取氨气 B.用装置乙除去氨气中的水蒸气
C.用装置丙验证氨气具有还原性 D.用装置丁吸收尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于材料的说法不正确的是
A.水泥是生活中常见的硅酸盐材料
B.二氧化硅是制造光导纤维的主要原料
C.不锈钢属于一种铁合金
D.纤维素是蚕丝的主要成分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列各组离子在指定溶液中能大量共存的是 ( )
A. 在无色溶液中: Na+ 、Fe3+、NO3- 、Cl-
B. pH=11的透明溶液中:Na+、K+、MnO4-、CO32-
C. 在含有HCO3-的溶液中:H+、K+、SO42-、Cl-
D. 含有大量Fe2+的溶液中:H+、K+、SO![]() 、NO
、NO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卷柏干枯后,如得到充足的水仍能成活,其原因是
A. 失去的水为自由水 B. 虽失去结合水,但有特殊酶
C. 此生物有特殊的结构 D. 以上都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使红色湿润石蕊试纸变蓝的气体,它们之间能发生如下反应:
①A+H2O―→B+C ②C + F―→D
③D+NaOH![]() F+E+H2O
F+E+H2O
(1)写出它们的化学式:
C________,D________,E________。
(2)写出各步反应的离子方程式:
①_______________________________________________________________;
③_______________________________________________________________。
(3)工业生产C的过程中有如下一步反应,即F经催化氧化生成B和H2O。写出该步反应的化学方程式:____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明乙酸是弱酸的实验事实是
A.CH3COOH溶液与Zn反应放出H2
B.0.1mol/L CH3COONa溶液的pH大于7
C.CH3COOH溶液与NaCO3反应生成CO2
D.0.1 mol/L CH3COOH溶液可使紫色石蕊变红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫的化合物在生产生活中有广泛应用。
(1)硫化钠主要用于皮革、毛纺、高档纸张、染料等行业。生产硫化钠大多采用无水芒硝(Na2SO4)-炭粉还原法,其流程示意图如下:

① 上述流程中采用稀碱液比用热水更好,理由是__________________。
② 取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌。若反应后测得溶液的pH=4,则此时溶液中c( S2-)=______mol·L-1。(已知:常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20)
(2)工业上常利用废碱渣(主要成分Na2CO3)吸收硫酸厂尾气中的SO2制备无水Na2SO3。KIO3滴定法可测定成品中Na2SO3的含量:室温下将0.1260g 成品溶于水并加入淀粉做指示剂,再用0.01000 mol·L1 KIO3酸性标准溶液滴定至终点,消耗KIO3溶液31.25mL。
① 滴定终点观察到的现象为:_____________________。
② 成品中Na2SO3的质量分数是_________(请写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com