
| A. | 分子里含有碳碳三键的不饱和链烃叫炔烃 | |
| B. | 炔烃分子里的所有碳原子都在同一直线上 | |
| C. | 炔烃易发生加成反应,也易发生取代反应 | |
| D. | 炔烃不能使溴水褪色,但可以使高锰酸钾酸性溶液褪色 |
分析 A.炔烃为分子中含有碳碳三键的碳氢化合物的总称;
B.碳链较长的炔烃分子中,碳原子不在一条直线上,呈折线型;
C.炔烃易发生加成反应,难发生取代反应;
D.炔烃既能使溴水褪色,也可以使高锰酸钾酸性溶液褪色.
解答 解:A.分子中含有碳碳三键的碳氢化合物为炔烃,故A正确;
B.多碳原子的炔烃中碳原子不一定在一条直线上,如丙炔中碳原子不在同一直线上,是折线形,1-丁炔中的4个碳原子不在同一直线上,故B错误;
C.炔烃含有碳碳三键易发生加成反应,难发生取代反应,故C错误;
D.炔烃含有碳碳三键易与溴单质发生加成反应使溴水褪色,碳碳三键也可以被高锰酸钾酸性溶液氧化,高锰酸钾酸性溶液褪色,故D错误.
故选A.
点评 本题考查炔烃的性质,题目难度不大,注意根据炔烃中含有三键判断炔烃的性质.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:解答题
 氯化铁是实验室中的重要试剂.某同学用m g含有铁锈(Fe2O3)的废铁屑来制取FeCl3•6H2O晶体,同时测定废铁屑中铁的质量分数,为此设计了如下装置(夹持装置略,气密性已检验):
氯化铁是实验室中的重要试剂.某同学用m g含有铁锈(Fe2O3)的废铁屑来制取FeCl3•6H2O晶体,同时测定废铁屑中铁的质量分数,为此设计了如下装置(夹持装置略,气密性已检验):查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:3:1 | B. | 1:3:2 | C. | 2:3:3 | D. | 3:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | W | |||
| Y | Z |
| A. | X元素形成的氢化物液态比固态的密度小 | |
| B. | 四种元素行成的简单离子半径从大小的排列顺序Y>Z>X>W | |
| C. | 常温下,Y形成的简单离子和W形成的简单离子在水溶液中可以大量共存 | |
| D. | Y常用于冶炼难熔的金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
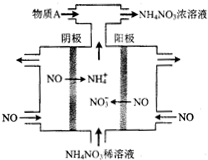
| A. | NO是常见的大气污染物之一,该装置可实现废气的治理与回收利用 | |
| B. | 阳极反应为:NO-3e-+2H2O═NO3-+4H+ | |
| C. | 阴极反应为:NO+5e-+6H+═NH4++H2O | |
| D. | 为使电解产物全部转化为NH4NO3,需向该电解池中补充水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com