
| A. | ①③④ | B. | 只有①④ | C. | 只有②③ | D. | 只有③④ |
分析 ①钠和水反应生成氢氧化钠,氢氧化钠与氯化亚铁反应生成不稳定的氢氧化亚铁,易被氧化生成氢氧化铁;
②向AlCl3溶液中逐滴加入过量的稀氢氧化钠溶液,得到偏铝酸钠;
③向饱和Na2CO3溶液中通入过量CO2,可得到碳酸氢钠;
④向NaAlO2溶液中通入过量CO2,生成氢氧化铝沉淀.
解答 解:①钠和水反应生成氢氧化钠,氢氧化钠与氯化亚铁反应生成不稳定的氢氧化亚铁,易被氧化生成氢氧化铁,为红褐色沉淀,故错误;
②向AlCl3溶液中逐滴加入过量的稀氢氧化钠溶液,得到偏铝酸钠,没有沉淀生成,故错误;
③向饱和Na2CO3溶液中通入过量CO2,可得到碳酸氢钠,由于碳酸氢钠的溶解度较小,可得到沉淀,故正确;
④向NaAlO2溶液中通入过量CO2,生成氢氧化铝沉淀,氢氧化铝不溶液碳酸,故正确.
故选D.
点评 本题考查了物质间的反应,为高频考点和常见题型,明确物质的性质是解本题关键,根据物质的性质来分析解答,熟练掌握元素化合物之间的反应,题目难度不大


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:选择题
| A. | CaCO3的电离方程式:CaCO3═Ca2+CO32- | |
| B. | NaHS水解:HS-+H2O═H3O++S2- | |
| C. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| D. | 用少量氨水吸收工业尾气中的SO2:2NH3•H2O+SO2═2NH4++SO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ•mol-1 | 436 | a | 945 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 光束穿过胶体时形成一条光亮的“通路” | |
| B. | 胶体粒子直径大小在1~100nm之间 | |
| C. | 胶体粒子可以透过滤纸 | |
| D. | 胶体粒子带有一定数目的电荷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有① | B. | ①和③ | C. | ①②③⑤ | D. | ①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 mol•L-1 的Na2SO4溶液中含有4 NA个Na+ | |
| B. | 将含有0.1 mol FeCl3的饱和溶液逐滴滴入足量沸水中,得到Fe(OH)3胶体数目为0.1 NA | |
| C. | 在标准状况下,11.2 L氖气中含有NA个氖原子 | |
| D. | 7.8 g Na2O2中阴离子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚中加入Na2CO3溶液中:CO32-+C6H5OH→C6H5O-+HCO3- | |
| B. | 0.3molFeI2与0.4molCl2在溶液中反应:6Fe2++10I-+8Cl2═6Fe3++16Cl-+5I2 | |
| C. | NaHSO4溶液与Ba(OH)2溶液反应后溶液呈中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| D. | AgCl固体溶于足量氨水:Ag++2NH3•H2O═[Ag(NH3)2]++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数为 8、中子数为 10 的氧原子:${\;}_{8}^{10}$O | |
| B. | 过氧化钠的电子式: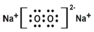 | |
| C. | 氧原子的电子排布图:1s22s22p4 | |
| D. | 次氯酸的结构式:H-Cl-O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
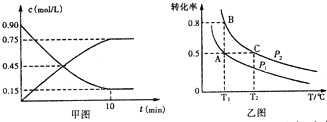
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com