
【题目】氮元素可以形成多种化合物。回答以下问题:
(1)基态氮原子的价电子排布式是___________________。
(2)C、N、O三种元素第一电离能从大到小的顺序是____________________
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被—NH2(氨基)取代形成的另一种氮的氢化物。
①NH3分子的空间构型是________________;N2H4分子中氮原子轨道的杂化类型是_________________。
②氨易溶于水的原因是__________________(写出两点即可)
③肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在________ (填标号)。
a.离子键 b.共价键 c.配位键 d.范德华力
(4)HCN的空间构型为_______
(5)尿素的化学式为CO(NH2)2,则碳原子的杂化轨道类型为__________________
【答案】 2s22p3 N>O>C 三角锥形 sp3 氨和水都是极性分子,相似相容;氨与水分子间可形成氢键;氨与水可发生反应(任意两点即可) d 直线 sp2
【解析】(1)基态氮原子的原子序数是7,则其价电子排布式是2s22p3;(2)非金属性越强,第一电离能越大,但氮元素的2p轨道电子处于半充满状态,稳定性强,所以C、N、O三种元素第一电离能从大到小的顺序是N>O>C;(3)①NH3分子中价层电子对数=![]() ,含有一对孤对电子,所以氨气的空间构型是三角锥形;肼(N2H4)分子可视为NH3分子中的一个氢原子被—NH2(氨基)取代形成的另一种氮的氢化物,所以根据氨气的结构可判断N2H4分子中氮原子轨道的杂化类型是sp3;②氨和水都是极性分子,相似相容,氨与水分子间可形成氢键,氨与水可发生反应,所以氨易溶于水;③肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,由于硫酸铵中存在离子键、共价键和配位键,则N2H6SO4的晶体内不存在的是范德华力,答案选d;(4)HCN的结构式为H-C≡N,所以空间构型为直线形;(5)尿素的化学式为CO(NH2)2,碳氧之间形成双键,碳氮之间形成单键,则碳原子的杂化轨道类型为sp2。
,含有一对孤对电子,所以氨气的空间构型是三角锥形;肼(N2H4)分子可视为NH3分子中的一个氢原子被—NH2(氨基)取代形成的另一种氮的氢化物,所以根据氨气的结构可判断N2H4分子中氮原子轨道的杂化类型是sp3;②氨和水都是极性分子,相似相容,氨与水分子间可形成氢键,氨与水可发生反应,所以氨易溶于水;③肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,由于硫酸铵中存在离子键、共价键和配位键,则N2H6SO4的晶体内不存在的是范德华力,答案选d;(4)HCN的结构式为H-C≡N,所以空间构型为直线形;(5)尿素的化学式为CO(NH2)2,碳氧之间形成双键,碳氮之间形成单键,则碳原子的杂化轨道类型为sp2。


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】室温下,2H2(g)+ O2(g) ![]() 2H2O(l)+ 566kJ。下列说法错误的是
2H2O(l)+ 566kJ。下列说法错误的是
A. H2→H+H的过程需要吸收热量
B. 若生成2mol水蒸气,则放出的能量大于566 kJ
C. 2g氢气完全燃烧生成液态水所释放的能量为283kJ
D. 2mol氢气与1mol氧气的能量之和大于2mol液态水的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来甲醇用途日益广泛,越来越引起商家的关注,工业上甲醇的合成途径多种多样。现有实验室中模拟甲醇合成反应,在2 L密闭容器内,400 ℃时反应:CO(g)+2H2(g)![]() CH3OH(g) △H<0,体系中n(CO)随时间的变化如表:
CH3OH(g) △H<0,体系中n(CO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 5 |
n(CO)(mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 |

(1)上图中表示CH3OH的变化的曲线是___________________。
(2)用H2表示从0~2s内该反应的平均速率v(H2) =__________________。
(3)能说明该反应已达到平衡状态的是_________________。
a.v(CH3OH) =2v(H2) b.容器内压强保持不变
c.2v逆(CO) = v正(H2) d.容器内密度保持不变
(4)已知常温常压下1g液态甲醇燃烧生成CO2气体和液态水放出22.68kJ的热量,则该反应的热化学方程式为:__________________。CH3OH与O2的反应可将化学能转化为电能,其工作原理如图所示,图中CH3OH从_______________(填A或B)通入,b极的电极反应式是___________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能是理想的清洁能源。科学家通过化学方法使能量按人们所期望的形式转化,从而提高能源的利用率。
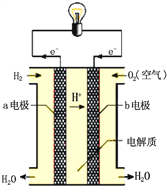
(1)氢气在燃烧时,放出大量热量,说明该反应是____反应(填“放热”或“吸热”);这是由于反应物的总能量___生成物的总能量(填“大于”或“小于”);从化学反应的本质角度来看,是由于断裂反应物中的化学键吸收的总能量________形成产物的化学键放出的总能量(填“大于”或“小于”)。
(2)通过氢气的燃烧反应,可以把氢气中蕴含的化学能转化为热能,如果将该氧化还原反应设计成原电池装置,就可以把氢气中蕴含的化学能转化为电能,右图就是能够实现该转化的装置,被称为氢氧燃料电池。
该电池的正极是_____(填“a电极”或“b电极”),在负极发生的电极反应式是_________________。电池反应的总方程式________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既属于非氧化还原反应,又属于吸热反应的是( )
A. 铝片和稀盐酸反应B. Ba(OH)28H2O与NH4Cl的反应
C. 灼热的碳与二氧化碳的反应D. 甲烷在氧气中的燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在酸性溶液中能大量共存而且为无色透明的溶液是
A.NH4+、Al3+、SO42-、NO3- B.K+、Fe2+、NO3-、SO42-
C.K+、MnO4-、NH4+、NO3- D.Na+、K+、ClO-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“碳呼吸电池”是一种新型能源装置,其工作原理如下图。下列说法正确的是

A. 该装置是将电能转变为化学能
B. 正极的电极反应为:C2O42--2e-=2CO2
C. 每得到1 mol草酸铝,电路中转移3 mol电子
D. 利用该技术可捕捉大气中的CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com