
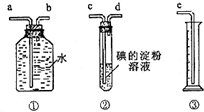
 某化学兴趣小组,模拟测定硫酸工业生产中SO2、N2和O2混合气体中SO2的体积分数,选用了下列简易实验装置:
某化学兴趣小组,模拟测定硫酸工业生产中SO2、N2和O2混合气体中SO2的体积分数,选用了下列简易实验装置:| 22.4 |
| 320 |


科目:高中化学 来源: 题型:
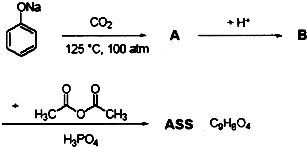
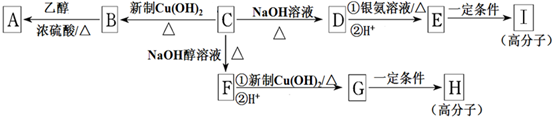
 耗NaOH溶液的体积,分别计算乙酰水杨酸的质量分数.在上述测定过程中,为防止乙酰水杨酸在滴定过程中水解,应如何正确操作?并说明理由.
耗NaOH溶液的体积,分别计算乙酰水杨酸的质量分数.在上述测定过程中,为防止乙酰水杨酸在滴定过程中水解,应如何正确操作?并说明理由.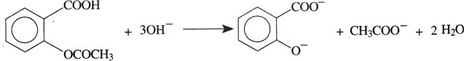
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若使溶液恢复到电解前的浓度可以向溶液中加20(10-b-10-a) g CuCO3 |
| B、?b<a<7 |
| C、阳极电极反应:2H2O-4e-═O2↑+4H+ |
| D、整个过程中是阳极产生氧气,阴极析出铜单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
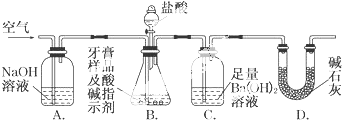
查看答案和解析>>
科目:高中化学 来源: 题型:
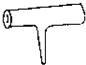 实验室里常见到如图所示仪器,该仪器为两头密封的玻璃管,中间带有一根玻璃短柄.该仪器可进行多项实验.当玻璃管内装有碘晶体时,用此仪器可进行碘升华实验,具有装置简单、操作方便、现象明显、没有污染,可反复使用等优点.
实验室里常见到如图所示仪器,该仪器为两头密封的玻璃管,中间带有一根玻璃短柄.该仪器可进行多项实验.当玻璃管内装有碘晶体时,用此仪器可进行碘升华实验,具有装置简单、操作方便、现象明显、没有污染,可反复使用等优点.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用过滤法分离Fe(OH)3胶体和FeCl3溶液的混合物 |
| B、用结晶法提纯NaCl和KNO3的混合物中的KNO3 |
| C、用蒸馏法分离乙醇和苯酚的混合物 |
| D、除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 测定次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| V(mL) | 25.40 | 22.10 | 21.90 | 22.00 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com