
�ϳɰ������Ĵ����������˹��̵�����Ҫ;�������о�������ȷ������ָ�����ϳɰ���Ӧ��ƽ�ⳣ��Kֵ���¶ȵĹ�ϵ���£�
| �� �ȣ��棩 | 360 | 440 | 520 |
| Kֵ | 0��036 | 0��010 | 0��0038 |
 CO(g) + 3H2(g) ��ȡ����֪�÷�Ӧ�У�����ʼ������е�
CO(g) + 3H2(g) ��ȡ����֪�÷�Ӧ�У�����ʼ������е� 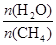 �㶨ʱ���¶ȡ�ѹǿ��ƽ������CH4������Ӱ������ͼ��ʾ��
�㶨ʱ���¶ȡ�ѹǿ��ƽ������CH4������Ӱ������ͼ��ʾ��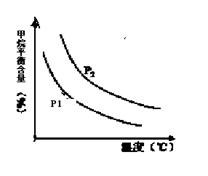
 CO2 (g) + H2(g) ��ȡ��
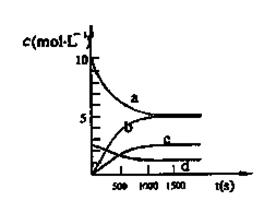
CO2 (g) + H2(g) ��ȡ����1�������¶����ߣ���Ӧ��ƽ�ⳣ��K��С ��a��d
��2���� < ������
��3���� 60 % �� 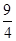 ��2��25 �� c��d
��2��25 �� c��d
�������������
��1���ٹ۲��������¶ȵ�����K��С����֪�÷�ӦΪ���ȷ�Ӧ��������ƽ��ʱH2��ת���ʣ��ı�������ƽ�������ƶ������Լ�ѹ�����£�����N2��Ũ�ȣ���С������Ũ�ȣ����Դ�a��d���ԡ�
��2������ͼ���֪���㶨�¶�ʱ�� P2���Ӧ��CH4��������P1�㣬���ɷ�Ӧ���ص㣬CH4(g) + H2O (g) CO(g) + 3H2(g)�����������������ѹǿԽ��CH4����Խ�ߣ����ԣ�P1<P2���ں㶨ѹǿʱ���¶�Խ�ߣ�CH4����Խ�ͣ��÷�ӦΪ���ȷ�Ӧ��
CO(g) + 3H2(g)�����������������ѹǿԽ��CH4����Խ�ߣ����ԣ�P1<P2���ں㶨ѹǿʱ���¶�Խ�ߣ�CH4����Խ�ͣ��÷�ӦΪ���ȷ�Ӧ��
��3����CO����ʼŨ��Ϊ0��2 mol��L-1��?c=0��2 mol��L-1-0��08 mol��L-1=0��012 mol��L-1������CO��ת����Ϊ0��012/0��2=0��6�� �÷�Ӧ�ĸ����ʵ�ƽ��Ũ��Ϊ[CO]= [H2O]=0��08 mol��L-1; [CO2] ="[" H2]=0��12 mol��L-1,����K=0��12��0��12/0��08��0��08=9/4=2��25��
�ڶ��ڸ÷�Ӧ����������ѹǿ�����������ܶ�ʼ�ղ���ʱ��ı䣬ab����
c����λʱ��������a mol CO2��ͬʱ����a mol H2������v��=v�棬��ȷ��d���ı�ˮ������CO�ij�ʼ���ʵ���֮�ȣ���n (CO) : n (H2O) : n (CO2) : n (H2)��1 : 16 : 6 : 6ʱ��Q=K�ﵽƽ��״̬��
���㣺��ѧ��Ӧ���ȵĿ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
����̼ѭ������������ĸ߶����ӣ���֪ú������ȿ�����ˮ������Ӧ������CO��H2Ϊ���ĺϳ������ϳ����й㷺Ӧ�á��Իش��������⣺
(1)��¯������CO�������Ҫ��;֮һ���������ӦΪ��FeO(s)��CO(g) Fe(s)��CO2(g) ��H��0����֪��1 100 ��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��K=0.263��
Fe(s)��CO2(g) ��H��0����֪��1 100 ��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��K=0.263��
���¶����ߣ���ѧƽ���ƶ���ﵽ�µ�ƽ�⣬��ʱƽ�ⳣ��Kֵ (���������С�����䡱)��
��1 100 ��ʱ��ø�¯�У�c(CO2)="0.025" mol��L-1��c(CO)="0.1" mol��L-1��������������£��÷�Ӧ�� ����(����ҡ�)���ж������� ��
(2)Ŀǰ��ҵ��Ҳ����CO2������ȼ�ϼ״����йط�ӦΪ��CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ��H����49.0 kJ��mol-1���������Ϊ1 L���ܱ������У�����1 mol CO2��3 mol H2����Ӧ�����в��CO2��CH3OH(g)��Ũ����ʱ��ı仯��ͼ��ʾ��
CH3OH(g)+H2O(g) ��H����49.0 kJ��mol-1���������Ϊ1 L���ܱ������У�����1 mol CO2��3 mol H2����Ӧ�����в��CO2��CH3OH(g)��Ũ����ʱ��ı仯��ͼ��ʾ��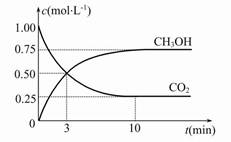
�ٴӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v(H2)�� ��
�ڷ�Ӧ�ﵽƽ������д�ʩ��ʹ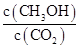 ������� (�����)��
������� (�����)��
| A�������¶� | B���ٳ���H2 | C���ٳ���CO2 | D����H2O(g)����ϵ�з��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
һ���¶��£���2L�ܱ�������NO2��O2�ɷ������з�Ӧ�� 4NO2(g)+O2(g)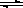 2N2O5(g)+5286 kJ��֪��ϵ��n(NO2)��ʱ��仯���±���
2N2O5(g)+5286 kJ��֪��ϵ��n(NO2)��ʱ��仯���±���
| t(s) | 0 | 500 | 1000 | 1500 |
| n(NO2)(mol) | 20 | 13.96 | 10.08 | 10.08 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ѧ��Ӧԭ���ڿ��к��������й㷺Ӧ�á�
����ͼװ����ʾ��A��B�еĵ缫Ϊ��Ķ��Ե缫��C��DΪ���ڽ���Na2SO4��Һ����ֽ���ϵIJ��У���Դ��a��b��������A��B�г���KOH��Һ������KOH��Һ��ˮ���С��ж�K1���պ�K2��K3ֱͨ���硣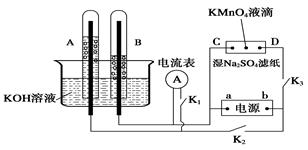
�ش��������⣺
��1�� a�ǵ�Դ�� ����д��A�еĵ缫��ӦʽΪ_____��
��2��ʪ��Na2SO4��ֽ�����ܹ۲쵽��������____________��
��3�����һ��ʱ���A��B�о��������Χ�缫������ʱ�ж�K2��K3���պ�K1�����ֵ�������ָ���ƶ���д����ʱB�еĵ缫��ӦʽΪ ��
�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������ҵ��һ��������з�Ӧ�ϳɼ״���CO(g)��2H2(g)  CH3OH(g) ��H���±����������Ǹ÷�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ��(K)����ش��������⣺
CH3OH(g) ��H���±����������Ǹ÷�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ��(K)����ش��������⣺
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
������(Si3N4)��һ�������մɲ��ϣ�������ʯӢ�뽹̿�ڸ��µĵ������У�ͨ�����·�Ӧ�Ƶã�3SiO2(s)+6C(s)+ 2N2(g)  Si3N4(s) + 6CO(g)
Si3N4(s) + 6CO(g)
��1���÷�Ӧ���������� ��2molN2�μӷ�Ӧת�Ƶ�����Ϊ ��
��2���÷�Ӧ��ƽ�ⳣ������ʽΪK������������ ����
��3����CO����������Ϊv(CO)��18mol��L-1��min-1����N2����������Ϊv(N2)��
��4���ﵽƽ��ı�ijһ������������ı�N2��CO����������Ӧ����v��ʱ��t�Ĺ�ϵ��ͼ��ͼ��t4ʱ����ƽ���ƶ������������� ��ͼ�б�ʾƽ��������CO�ĺ�����ߵ�һ��ʱ���� ��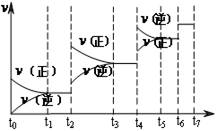
��5�����÷�Ӧ��ƽ�ⳣ��Ϊ K��729������ͬ�¶���1L�ܱ������У�������SiO2��C��2mol N2��ַ�Ӧ����N2��ת������ (��ʾ��272 = 729)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�α���ͨ������ᣨH2C2O4����Һ�еμ��������ữ����������о�Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬����д���÷�Ӧ�Ļ�ѧ����ʽ ���÷�Ӧ����ʹ��ָʾ����ԭ���� ��
��ijͬѧ���ݿα���������Ի�ѧ��Ӧ���ʵ�Ӱ��ԭ�����������������������ᷴӦ�й�ʵ�飬ʵ����̵����ݼ�¼���£����������ϱ�����Ϣ���ش��й����⣺
| ʵ�� ��� | ��Ӧ�¶� ���棩 | �μӷ�Ӧ������ | ||||
| Na2S2O3 | H2SO4 | H2O | ||||
| V/mL | c/mol?L-1 | V/mL | c/mol?L-1 | V/mL | ||
| A | 20 | 10 | 0��1 | 10 | 0��1 | 0 |
| B | 20 | 5 | 0��1 | 10 | 0��1 | 5 |
| C | 20 | 10 | 0��1 | 5 | 0��1 | 5 |
| D | 40 | 5 | 0��1 | 10 | 0��1 | 5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
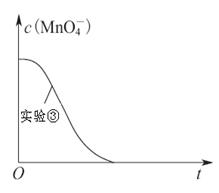
ijС������H2C2O4��Һ������KMnO4��Һ��Ӧ��̽������������Ի�ѧ��Ӧ���ʵ�Ӱ�족��ʵ��ʱ���ȷֱ���ȡ������Һ��Ȼ�����Թ���Ѹ����Ͼ��ȣ���ʼ��ʱ��ͨ���ⶨ��ɫ����ʱ�����жϷ�Ӧ�Ŀ�������С����������·�����
| ʵ���� | H2C2O4��Һ | ����KMnO4��Һ | �¶� | ||
| Ũ��(mol·L��1) | ���(mL) | Ũ��(mol·L��1) | ��� (mL) | ||
| �� | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| �� | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| �� | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��֪��ӦA��g��+B(g) C(g)+D(g)��H��0�ش��������⣺
C(g)+D(g)��H��0�ش��������⣺
��1���÷�Ӧ��________��Ӧ������ȡ����ȡ���
��2������Ӧ�ﵽƽ��ʱ�������¶ȣ�A��ת����________���������С�����䡱����ԭ����________________________________________��
��3����Ӧ��ϵ�м���������Է�Ӧ���Ƿ���Ӱ�죿________��ԭ����_________________________________________________��
��4����Ӧ��ϵ�м����������Ӧ����________���������С�����䡱������Ӧ�Ļ��________���������С�����䡱����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
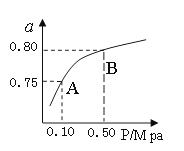
�״�����Ҫ�Ļ�ѧ��ҵ����ԭ�Ϻ����Һ��ȼ�ϡ���ҵ�Ͽ�����CO��CO2������ȼ�ϼ״�����֪�״��Ʊ����йػ�ѧ��Ӧ�Լ��ڲ�ͬ�¶��µĻ�ѧ��Ӧƽ�ⳣ�����±���ʾ��
| ��ѧ��Ӧ | ƽ�ⳣ�� | �¶ȡ� | |
| 500 | 800 | ||
��2H2(g)+CO(g) CH3OH(g) CH3OH(g) | K1 | 2.5 | 0.15 |
��H2(g)+CO2(g) H2O (g)+CO(g) H2O (g)+CO(g) | K2 | 1.0 | 2.50 |
��3H2(g)+CO2(g) CH3OH(g)+H2O (g) CH3OH(g)+H2O (g) | K3 | | |


�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com