
����Ŀ�����ú�̼������ϳ�ȼ���ǽ����ԴΣ������Ҫ��������֪CO��g��+2H2��g��CH3OH��g����Ӧ�����е������仯�����ͼ��ʾ�����ߢ�����ߢ�ֱ��ʾ��ʹ�ô�����ʹ�ô�������������������ж���ȷ���ǣ� �� 
A.�÷�Ӧ�ġ�H=+91 kJmol��1
B.����������÷�Ӧ�ġ�H��С
C.��Ӧ���������С���������������
D.����÷�Ӧ����Һ̬CH3OH�����H��С
���𰸡�D
���������⣺A����Ӧ���������������������������÷�Ӧ���ȣ���A����
B����������������˷�Ӧ�Ļ�ܣ�����Ӧ�������������û�䣬���������H���䣬��B����
C����ͼ���֪����Ӧ������������������������������C����
D������÷�Ӧ����Һ̬CH3OH���ų��������������Ӧ��Ϊ��ֵ�����H��С����D��ȷ��
��ѡD��
�����㾫�������ڱ��⿼��ķ�Ӧ�Ⱥ��ʱ䣬��Ҫ�˽��ڻ�ѧ��Ӧ�зų������յ�������ͨ���з�Ӧ�Ȳ��ܵó���ȷ�𰸣�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ������K�������ƶ������г���2mol A��1mol B�����г���2mol C��1mol He����ʱKͣ��0����������Ӧ2A��g��+B��g��2C��g�����ﵽƽ��ָ����¶ȣ������й�˵������ȷ����
�� ��
A.��ƽ�����K����ͣ�������̶�0��2֮��
B.��ƽ��ʱKͣ�������1���������ͣ�����Ҳ�6��
C.�ﵽƽ��ʱ����������B�����ʵ���С������������B�����ʵ���
D.���ݸ���K���������ж��������ߵķ�Ӧ�Ƿ�ﵽƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������е������ǽ����ѧ���ⷽ������Ҫ;���������ݵ����������ȷ����
A.���û�ѧƽ�ⳣ���жϻ�ѧ��Ӧ���еĿ���
B.�����ܽ�������ж�������ԭ��Ӧ�����Ŀ�����
C.���÷е������Ʋ⽫һЩҺ���������Ŀ�����
D.�������ʵ�Ħ�������ж���ͬ״̬�²�ͬ�����ܶȵĴ�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ѽⷨ������ҵ�������ԭ��Ϊ��2H2SO4��l��=2SO2��g��+O2��g��+2H2O��g����H=+550kJ/mol������������Ӧ��ɣ�
i��H2SO4��l��=SO3��g��+H2O��g����H=+177kJ/mol
ii��SO3��g���ֽ⣮
��1��SO3��g���ֽ���Ȼ�ѧ����ʽΪ
��2����ҵ�ϳ���SO2�Ʊ�Na2S2O3 �� ��0.1mol/L��Na2S2O3��Һ�еμ�ϡ��������ӷ���ʽΪ ��
��3����Ӧii�ġ�S0 �������������������=������
��4���Է�Ӧii������V2O5�������� ��֪��SO2+V2O5SO3+V2O4K1�� ![]() O2+V2O4V2O5K2 �� ������ͬ�¶��£�2SO3��g��2SO2��g��+O2��g����ƽ�ⳣ�� K=����K1��K2��ʾ����
O2+V2O4V2O5K2 �� ������ͬ�¶��£�2SO3��g��2SO2��g��+O2��g����ƽ�ⳣ�� K=����K1��K2��ʾ����
��5��L��L1��L2����X�ɷֱ����ѹǿ���¶ȣ���ͼ��ʾLһ��ʱ����Ӧii��SO3��g����ƽ��ת������X�ı仯��ϵ�� 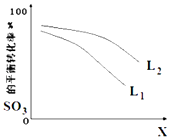
��X����������������
�ڱȽ�L1��L2�Ĵ�С ��
��6��ά����ϵ��ѹp�㶨����T��ʱ�����ʵ���Ϊ9mol�����Ϊ2L��SO3��g��������Ӧ��2SO3��g��2SO2��g��+O2��g������֪SO3��ƽ��ת����25%�����ڸ��¶��·�Ӧ��ƽ�ⳣ��K=������������ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״���£���22.4L HCl��ȫ����1Lˮ�У�ˮ���ܶȽ���Ϊ1g/mL������Һ���ܶ�Ϊ�� g/cm3 �� ��Һ�����ΪV mL�����ʵ���������Ϊw�����ʵ����ʵ���Ũ��Ϊc mol/L��������������ȷ���ǣ� ��
��w= ![]() ��100% c=1molL��1 ��������Һ���ټ���V mLˮ��������Һ��������������0.5w ������Һ�к���NA��HCl���ӣ�
��100% c=1molL��1 ��������Һ���ټ���V mLˮ��������Һ��������������0.5w ������Һ�к���NA��HCl���ӣ�
A.ȫ��
B.�٢ۢ�
C.�٢�
D.ֻ�Т�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2008��5�£��ҹ��Ĵ����������ش�����ֺ��������������ˮ������ɱ����Ϊ���ƴ��ģ��Ⱦ�Լ�����������Ч����֮һ��������Cl2�����Ʊ�����������Ҫԭ��֮һ����ҵ����Ҫ���õ�ⱥ��ʳ��ˮ�ķ�������ȡCl2����ش��������⣺
��1�����֮ǰ��ʳ��ˮ��Ҫ���ƣ�Ŀ���dz�ȥ���ε��е�Ca2+��Mg2+��SO42-���������ӣ�ʹ�õ��Լ��У���Na2CO3��Һ ��Ba(OH)2��Һ ��ϡ���ᡣ���к����ļ���˳��Ϊ___�����������
��2��ʵ����������6.00 mol/L��ʳ��ˮ90 mL���ش��������⣺
����Ҫ������NaCl___________________g��
�ڿɹ�ѡ��������У�a������ b��ƿ c�ձ� d��ͷ�ι� e�Թ� f������ƽ������ hҩ�ס�������ʳ��ˮʱ����Ҫʹ�õ���_______������ĸ������ȱ�ٵ�������__________��
��������Һʱ��һ����Է�Ϊ���¼������裺���������ܽ���________________________��ת����_____________________��������__________________________��װƿ��
�����в�����ʹ������Һ��Ũ��ƫС����___________________��
A. ת������Һ��δϴ�Ӳ��������ձ� B. ����ƿ��ԭ������������ˮ
C. ����ʱ�����ӿ̶��� D. �����Ȼ��ƹ���ʱ��������
��3���ڵ�ⱥ��ʳ��ˮ�����У���������H2��NaOH������������Ӧ�Ļ�ѧ��Ӧ����ʽΪ_____________________________��
��4����������ɵ�Cl2ͨ��NaOH��Һ�����������Σ�����һ��������Һ����Ҫ�ɷ�NaClO��Ӧ��������ԭ��Ӧԭ����д���˷�Ӧ�Ļ�ѧ����ʽ��_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����50mL NaNO3��Na2SO4�Ļ����Һ�У�c ��Na+��=1mol/L�������м�������BaCl2��Һǡ����ȫ��Ӧ���õ�2.33g��ɫ��������ԭ�����Һ��c ��NO3����=mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���20.00mL 0.1000molL��1 ��NH4��2SO4��Һ����μ���0.2000molL��1 NaOHʱ����Һ��pH������NaOH��Һ����Ĺ�ϵ��ͼ��ʾ�������ǻӷ���������˵����ȷ���ǣ� �� 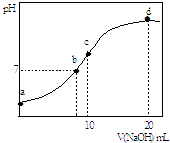
A.��a��ʾ��Һ�У�c��SO42������c��NH4+����c��H+����c��OH����
B.��b��ʾ��Һ�У�c��NH4+��=c��Na+����c��H+��=c��OH����
C.��d��ʾ��Һ�У�c��SO42������c��NH3H2O ����c��OH������c��NH4+��
D.��c��ʾ��Һ�У�c��SO42����+c��H+��=c��NH3H2O ��+c��OH����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com