


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 元素编号 | T | X | Y | Z | W |
| 元素的性质或原子结构情况 | 短周期主族元素中原子半径最大 | 最外层上的电子数比次外层少1个且单质是气体 | 核外共有13种运动状态不同的电子 | 若低温蒸发液态空气,因其沸点较低可先获得它的单质 | 核外有5种不同能量的电子且其中有两个未成对的电子 |

查看答案和解析>>
科目:高中化学 来源:2012-2013学年上海市浦东新区高三下学期三模考试化学试卷(解析版) 题型:填空题
现有部分短周期主族元素的有关信息,如下表:
|
元素编号 |
T |
X |
Y |
Z |
W |
|
元素的性质或原子结构情况 |
短周期主族元素中原子半径最大 |
最外层上的电子数比次外层少1个且单质是气体 |
核外共有13种运动状态不同的电子 |
若低温蒸发液态空气,因其沸点较低可先获得它的单质 |
核外有5种不同能量的电子且其中有两个未成对的电子 |
(1)Y的最外层电子排布式是__ __,它的单质与碳生成的化合物与水反应生成甲烷和白色沉淀。写出该反应的化学方程式__ 。
(2)元素T的单质与水反应的离子方程式是 ,
在短周期主族元素中,X元素与其相邻元素的原子半径从小到大的顺序是_
(写元素符号)。
(3)W形成的一种单质,其式量为256,易溶于CS2,该单质的化学式为___ __,它属于_ ___晶体(写晶体类型)。
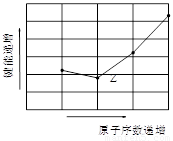
(4)如图为Z元素所在周期气态氢化物R-H键的键能大小,则该周期元素气态氢化物键能大小与键长的关系为___ __ (用文字简述)。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年福建省高三12月月考化学试卷 题型:选择题
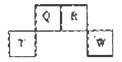
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等。X、Y也是短周期主族元素,且X+、Y2-的核外电子排布相同。下列说法错误的是

A.非金属性:Q <W
B.Q、R、W三种元素的常见单质中所含微粒间的作用力完全相同
C.原子半径:X>T;离子半径:X+<Y2-
D.T单质能与X的最高价氧化物的水化物反应
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com