
分析 ①同主族从上到下金属性增强;
②同主族从上到下非金属性减弱;
③同周期从左向右金属性减弱,金属性越强,对应最高价氧化物的水化物的碱性越强;
④同周期从左向右非金属性增强,非金属性越强,对应最高价氧化物的水化物的酸性越强;
⑤具有相同电子排布的离子,原子序数大的离子半径小;
⑥非金属性越强,对应氢化物越稳定.
解答 解:①同主族从上到下金属性增强,则金属性Li<K,故答案为:<;
②同主族从上到下非金属性减弱,则非金属性:N>P,故答案为:>;
③同周期从左向右金属性减弱,金属性越强,对应最高价氧化物的水化物的碱性越强,则碱性:Mg(OH)2>Al(OH)3,故答案为:>;
④同周期从左向右非金属性增强,非金属性越强,对应最高价氧化物的水化物的酸性越强,酸性:H2CO3>H2SiO3,故答案为:>;
⑤具有相同电子排布的离子,原子序数大的离子半径小,则半径:F->Na+,故答案为:>;
⑥非金属性越强,对应氢化物越稳定,则稳定性:H2S<HCl,故答案为:<.
点评 本题考查元素周期表和周期律,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.


 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 排水法收集气体后,先熄灭酒精灯,再取出导气管 | |
| B. | 蒸馏自来水时,冷凝水从上口进,从下口出 | |
| C. | 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 | |
| D. | 稀释浓硫酸时,应将浓硫酸慢慢加入水中并及时搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验序号 | ① | ② | ③ | ④ |
| m(粉末样品)/g | 0.90 | 1.80 | 3.60 | 7.20 |
| m(反应后剩余固体)/g | 0 | 0.64 | 2.48 | 6.08 |
| A. | 实验①反应后溶液中含有Fe3+、Fe2+、Cu2+ | |
| B. | 实验②③反应后剩余固体全部是Cu | |
| C. | 实验④的滤液中c(Fe2+)=1.5 mol/L | |
| D. | 原粉末样品中m(Fe):m(Cu)=7:8 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 普通水泥在固化过程中自由水分子减少,并且溶液呈碱性.根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间.此法的原理如图所示,反应的总方程式为:2Cu+Ag2O=Cu2O+2Ag,下列有关说法正确的是( )
普通水泥在固化过程中自由水分子减少,并且溶液呈碱性.根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间.此法的原理如图所示,反应的总方程式为:2Cu+Ag2O=Cu2O+2Ag,下列有关说法正确的是( )| A. | 外电路上,电子由Cu电极沿导线流入Ag2O电极 | |
| B. | 测量原理示意图中,Ag2O为负极 | |
| C. | 负极的电极反应式为:2Cu+2OH--2e-=Cu2O+H2O | |
| D. | 电池工作时,OH-向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 根据如图反应框图填空.已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应.
根据如图反应框图填空.已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应.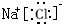
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,28g氮气的体积约为22.4升 | |
| B. | 标准状况下,11.2L水含有1mol氢原子 | |
| C. | 标准状况下,11.2L氧气与硫充分反应,转移的电子数目为2NA | |
| D. | 常温常压下,1mol氯气完全被碱吸收需要NA个氢氧根离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 |  | 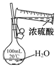 | 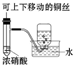 |
| A.制备少量氨气 | B.吸收HCl | C.配制一定浓度硫酸溶液 | D.制备并收集少量NO2气体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com