
有关短周期元素A、B、C、D、E、F的信息如下:
元素 有关信息
A 最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐
B 最外层电子数是次外层电子数的2倍
C M层上有3个电子
D 短周期原子半径最大的主族元素
E 其单质是淡黄色固体
F 最高正价与最低负价代数和为6
请回答下列问题:
(1)写出基态A原子外围电子的电子排布图 .气态氢化物乙中A原子的杂化类型是SP3.
(2)E、F两元素的电负性大小比较:E F(选填>、<或=)
(3)下列说法正确的是 (填序号).
①实验室可用右图所示装置制取B的最高价氧化物.
②用C单质做成的槽车,都可用来运输甲的浓溶液.
③C形成的单质熔点低于D形成的单质的熔点.
④E的氢化物稳定性强于F的氢化物稳定性.
(4)将E的常见氧化物(该氧化物能使品红溶液褪色)通入由CuSO4和NaCl混合的浓溶液中,溶液颜色变浅,析出白色沉淀,取该沉淀进行元素质量分数分析,可知其中含Cl:35.7%,Cu:64.3%,则该氧化物在上述反应中的作用是 .
A.漂白剂B.氧化剂C.还原剂.

考点: 位置结构性质的相互关系应用.
分析: A的最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐,则A为N元素,甲为HNO3、乙为NH3;B原子最外层电子数是次外层电子数的2倍,只能有2个电子层,最外层电子数为4,则B为碳元素;C元素原子M层上有3个电子,则C为Al;D是短周期原子半径最大的主族元素,则D为Na;E的单质是淡黄色固体,则E为硫元素;F元素的最高正价与最低负价代数和为6,处于ⅦA族,则F为Cl,据此解答.
解答: 解:A的最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐,则A为N元素,甲为HNO3、乙为NH3;B原子最外层电子数是次外层电子数的2倍,只能有2个电子层,最外层电子数为4,则B为碳元素;C元素原子M层上有3个电子,则C为Al;D是短周期原子半径最大的主族元素,则D为Na;E的单质是淡黄色固体,则E为硫元素;F元素的最高正价与最低负价代数和为6,处于ⅦA族,则F为Cl,
(1)A为氮元素,原子外围电子的电子排布图为 ,气态氢化物NH3中N原子的价层电子对数为
,气态氢化物NH3中N原子的价层电子对数为 =4,所以N原子杂化类型是SP3
=4,所以N原子杂化类型是SP3
杂化,
故答案为: ;SP3;
;SP3;
(2)E为硫元素、F为氯元素,根据元素周期律,它们的电负性大小比较:S<Cl,
故答案为:<;
(3)①B的最高价氧化物为二氧化碳,可以用碳酸钙与盐酸反应制备,反应为固体与液体反应且不需要加热,可以用图中装置制备,故正确;
②Al在浓硝酸中发生钝化现象,可以用Al单质制成的槽车,可用来运输硝酸浓溶液,故正确;
③Al的熔点高于Na的熔点,故错误;
④硫化氢稳定性弱于氯化氢的稳定性,故错误;
故选①②;
(4)将E的常见氧化物能使品红溶液褪色,该氧化物为二氧化硫,由Cl和Cu的百分含量知,沉淀中只含Cu和Cl两种元素(35.7%+64.3%=100%),且两者的物质的量之比约为 :
: =1:1,可知,其化学式为CuCl,其中Cu的化合价为+1价,则原反应物中CuSO4为氧化剂,那可能的还原剂只有SO2,氧化产物是SO42﹣,
=1:1,可知,其化学式为CuCl,其中Cu的化合价为+1价,则原反应物中CuSO4为氧化剂,那可能的还原剂只有SO2,氧化产物是SO42﹣,
故答案为:C;
点评: 本题考查结构性质位置关系应用,推断元素是解题关键,第(4)问,注意根据元素质量分数确定沉淀的组成,侧重对考查学生分析解决问题的能力,难度中等.


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
维生素C的结构简式如图所示。

(1)维生素C的分子式是________。
(2)维生素C________溶于水(填“易”或“难”)。
(3)在维生素C溶液中滴入紫色石蕊试液,溶液颜色变红,说明维生素C溶液具有________性。
(4)在维生素C溶液中滴入少量蓝色的含有淀粉的碘水,可观察到溶液蓝色退去,说明维生素C具有________性。
(5)中学生每天需补充约60 mg维生素C,下列物质中含有丰富维生素C的是________。
A.辣椒 B.鸡蛋 C.米饭 D.青霉素
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z是1~20号中的四种元素,原子序数依次增大。W的主要化合价为-2价,原子半径为0.074 nm;X所在的主族序数与所在的周期序数之差为3;Y原子最外层电子数为奇数;Z最高价氧化物对应的水化物电离出的阴、阳离子数目相等。下列说法正确的是 ( )。
A.W可能是氧元素,也可能是硫元素
B.X元素氧化物对应的水化物一定是一种强酸
C.Y元素原子次外层电子数与最外层电子数之差为1
D.Z可能是氯元素,也可能是钾元素
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是()
A. 分子晶体中一定不含离子键,但一定存在共价键
B. 金属与非金属元素形成的化合物一定是离子化合物
C. NCl3分子中所有的原子均为8电子稳定结构
D. NaHSO4晶体中阴、阳离子的个数比是1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族,其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9,单质Y可与NaOH溶液反应生成氢气.下列说法不正确的是()
A. 原子半径:Y>Z>W
B. XW2熔点为107℃,沸点为142.5℃,说明固态XW2为分子晶体
C. 电解YW3固体可得单质Y
D. 
ZW2分子结构见右图,说明ZW2是极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
现有三组混合液:①乙酸乙酯和乙酸钠溶液 ②乙醇和丁醇 ⑧溴化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
|
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 |
|
| C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
可用于鉴别以下三种化合物最合理的一组试剂是( )
①银氨溶液 ②溴的四氯化碳溶液 ③氯化铁溶液 ④氢氧化钠溶液
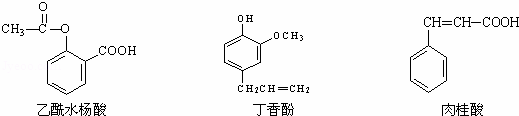
|
| A. | ②与③ | B. | ③与④ | C. | ①与④ | D. | ①与② |
查看答案和解析>>
科目:高中化学 来源: 题型:
将X气体通入BaCl2溶液,未见沉淀生成,然后通入Y气体,有沉淀生成,X、Y不可能是
| 选项 | X | Y |
| A | SO2 | H2S |
| B | Cl2 | CO2 |
| C | NH3 | CO2 |
| D | SO2 | Cl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com