
| A.d、e、f | B.b、d、e、f | C.b、d、e | D.b、c、e、f |
科目:高中化学 来源:不详 题型:填空题
 2SO3,在一定温度下,反应达到平衡,得到0.12 mol SO3,则反应的平衡常数K= 。若温度不变,再加入0.50 mol氧气后重新达到平衡,则SO2的平衡浓度 (填“增大”“不变”或“减小”),氧气的转化率 (填“升高”“不变”或“降低”),SO3的体积分数 (填“增大”“不变”或“减小”)。
2SO3,在一定温度下,反应达到平衡,得到0.12 mol SO3,则反应的平衡常数K= 。若温度不变,再加入0.50 mol氧气后重新达到平衡,则SO2的平衡浓度 (填“增大”“不变”或“减小”),氧气的转化率 (填“升高”“不变”或“降低”),SO3的体积分数 (填“增大”“不变”或“减小”)。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
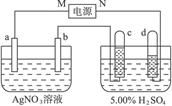
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铜一锌原电池中,铜是负极 |
| B.用电解法精炼粗铜时,粗铜作阴极 |
| C.在镀件上电镀铜时,用金属铜作阳极 |
| D.电解稀硫酸制H2、O2时,铜作阳极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
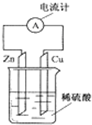
| A.反应物是锌和稀硫酸 |
| B.铜片上不产生气泡 |
| C.电流计显示导线上电子由锌片流向铜片 |
| D.该装置能将化学能转变为电能 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
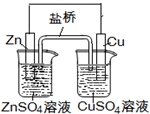
| A.电镀时,通常把待镀的金属制品作阴极 |
| B.氢氧燃料电池(酸性电解质)中O2通入负极 |
| C.图中电子由Cu极流向Zn,盐桥中的Cl-移向CuSO4溶液 |
| D.在海轮外壳镶嵌锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Zn为负极,MnO2为正极 |
| B.MnO2为正极,Zn为负极 |
| C.工作时电子由MnO2经外电路流向Zn极 |
| D.Zn电极发生还原反应,MnO2电极发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 2NH3(g).在一体积为10L且容积不变的密闭容器中放入1mol N2和3mol H2 ,在一定条件下发生反应,经4min达到化学平衡状态,测得容器中氨气的物质的量为0.6mol.。求:
2NH3(g).在一体积为10L且容积不变的密闭容器中放入1mol N2和3mol H2 ,在一定条件下发生反应,经4min达到化学平衡状态,测得容器中氨气的物质的量为0.6mol.。求:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com