
分析 设一氧化碳的浓度变化量为xmol/L,则:
CO(g)+H2O(g)?H2(g)+CO2(g)
起始量(mol/L):0.01 0.01 0 0
变化量(mol/L):x x x x
平衡量(mol/L):0.01-x 0.01-x x x
再根据平衡常数K=$\frac{c({H}_{2})×c(C{O}_{2})}{c(CO)×c({H}_{2}O)}$=9可计算x,进而计算各物质的反应速率、转化率等,以此解答该题.
解答 解:设一氧化碳的浓度变化量为xmol/L,则:
CO(g)+H2O(g)?H2(g)+CO2(g)
起始量(mol/L):0.01 0.01 0 0
变化量(mol/L):x x x x
平衡量(mol/L):0.01-x 0.01-x x x
则K=$\frac{c({H}_{2})×c(C{O}_{2})}{c(CO)×c({H}_{2}O)}$=$\frac{x×x}{(0.01-x)×(0.01-x)}$=9,解得:x=0.0075,
(1)从反应开始至达到平衡时CO的反应速率为$\frac{0.0075mol/L}{10min}$=7.5×10-4mol•L-1•min-1,故答案为:7.5×10-4;
(2)CO转化率=$\frac{0.0075mol/L}{0.01mol/L}$×100%=75%,
故答案为:75%;
(3)因反应前后气体的体积相等,则增大压强平衡不移动,在恒温恒容的条件下,向上述平衡体系中再充入等物质的量之比的CO(g)和H2O(g)重新达到平衡时,H2的体积百分数不变,为$\frac{0.0075}{0.02}×100%$=37.5%.
故答案为:37.5%.
点评 本题考查化学平衡有关计算,为高考常见题型,侧重于学生的分析能力和计算能力的考查,题目比较基础,注意三段式在化学平衡计算中应用,掌握化学平衡常数的用途:1、判断反应进行的程度,2、判断反应的热效应,3、判断反应进行的方向,4、计算转化率等.


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案科目:高中化学 来源: 题型:解答题
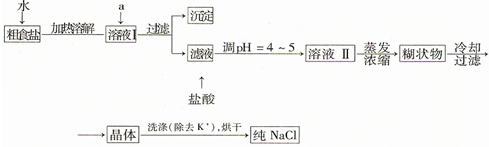
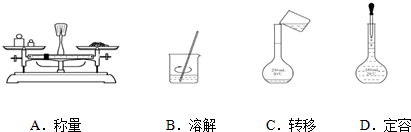
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
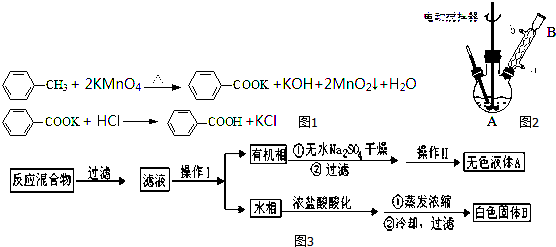
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| SO2的转化率% | 0.1MPa | 1MPa | 10MPa |
| 400°C | 99.2 | 99.7 | 99.9 |
| 600°C | 73.7 | 89.5 | 96.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
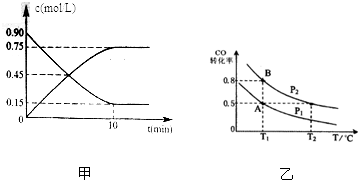
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 实验室用NaBr、浓H2SO4、乙醇为原料,制备溴乙烷,反应的化学方程式为:
实验室用NaBr、浓H2SO4、乙醇为原料,制备溴乙烷,反应的化学方程式为:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.5 mol•L-1•s-1 | B. | v(B)=0.5 mol•L-1•s-1 | ||
| C. | v(C)=1.8 mol•L-1•min-1 | D. | v(D)=1 mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
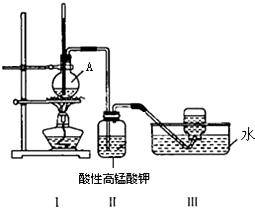 某学习小组在实验室里用乙醇与浓硫酸混合加热制乙烯,并进行有关乙烯性质的探究.装置如图.请帮助回答下列问题:
某学习小组在实验室里用乙醇与浓硫酸混合加热制乙烯,并进行有关乙烯性质的探究.装置如图.请帮助回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com