
C和CuO在高温下反应可能生成Cu、Cu2O、CO2、CO.现将1g碳粉跟8g CuO混合,在硬质试管中隔绝空气高温加热,将生成的气体全部通入足量NaOH溶液中,并收集残余的气体,测得溶液增加的质量为1.1g,残余气体在标准状况下的体积为560mL.下列说法错误的是()
A. 在硬质试管中隔绝空气高温加热固体混合物时,有0.6 g碳参加了反应
B. 试管中发生的所有氧化还原反应共转移电子0.15 mol
C. 反应后试管中剩余的固体混合物的总质量为7.2 g
D. 反应生成铜和氧化亚铜的总物质的量为0.1 mol
考点: 有关混合物反应的计算;铜金属及其重要化合物的主要性质.
分析: 生成的气体全部通过足量NaOH溶液,收集残余气体.测得溶液增重的1.1g为二氧化碳的质量,二氧化碳的物质的量为: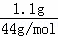 =0.025mol,残余气体在标准状况下的体积为560mL为CO的体积,一氧化碳的物质的量为:
=0.025mol,残余气体在标准状况下的体积为560mL为CO的体积,一氧化碳的物质的量为: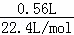 =0.025mol,
=0.025mol,
A.根据碳元素守恒可知参加反应的碳原子物质的量等于二氧化碳与一氧化碳的物质的量之和,根据m=nM计算参加反应的碳的质量;
B.反应中碳元素化合价升高,铜元素化合价降低,根据碳元素的化合价变化计算转移电子数目;
C.碳粉与CuO的总质量减去二氧化碳及一氧化碳的质量即为反应后的试管中固体混合物总质量;
D.根据氧原子守恒计算反应后试管中固体混合物含有的氧原子物质的量,进而计算氧化亚铜的物质的量,再根据铜元素守恒计算反应生成铜的物质的量.
解答: 解:生成的气体全部通过足量NaOH溶液,收集残余气体.测得溶液增重的1.1g为二氧化碳的质量,CO2的物质的量为: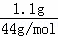 =0.025mol,残余气体在标准状况下560mL气体为CO的体积,则CO的物质的量为:
=0.025mol,残余气体在标准状况下560mL气体为CO的体积,则CO的物质的量为: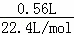 =0.025mol,
=0.025mol,
A.根据碳元素守恒可知:参加反应的C原子的物质的量等于CO2与CO的物质的量之和,所以参加反应的碳元素质量为:(0.025mol+0.025mol)×12g/mol=0.6g,故A正确;
B.反应中C元素化合价升高,铜元素化合价降低,所以转移电子物质的量为:0.025mol×4+0.025mol×2=0.15mol,故B正确;
C.生成的CO2和CO的总质量为:0.025mol×44g/mol+0.025mol×28g/mol=1.8g,所以反应后试管中固体混合物总质量为:(1g+8g)﹣1.8g=7.2g,故C正确;
D.氧化铜的物质的量为:n(CuO)= =0.1mol,二氧化碳与一氧化碳含有的氧原子物质的量为:0.025mol×2+0.025mol×1=0.075mol,反应后氧原子存在于氧化亚铜中,所以氧化亚铜的物质的量为:0.1mol﹣0.075mol=0.025mol,铜的物质的量为:0.1mol﹣0.025mol×2=0.05mol,反应生成铜和氧化亚铜的总物质的量为0.075mol,故D错误;
=0.1mol,二氧化碳与一氧化碳含有的氧原子物质的量为:0.025mol×2+0.025mol×1=0.075mol,反应后氧原子存在于氧化亚铜中,所以氧化亚铜的物质的量为:0.1mol﹣0.075mol=0.025mol,铜的物质的量为:0.1mol﹣0.025mol×2=0.05mol,反应生成铜和氧化亚铜的总物质的量为0.075mol,故D错误;
故选D.
点评: 本题考查混合物的计算,题目难度较大,试题综合性较强,解答关键是根据原子守恒进行计算,注意守恒思想在混合物计算的运用方法,试题有利于提高学生的分析、理解能力及化学计算能力.


科目:高中化学 来源: 题型:
下列措施或事实不能用勒沙特列原理解释的是( )
|
| A. | 滴加酚酞的氨水中加入氯化铵固体后红色变浅 |
|
| B. | 棕红色的NO2加压后颜色先变深后变浅(已知:2NO2 (g)⇌N2O4 (g)) |
|
| C. | 煅烧粉碎的硫铁矿利于SO2的生成 |
|
| D. | 工业上生产硫酸的过程中,使用过量的空气以提高SO2的利用率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液显酸性的是 ( )。
①pH<7的溶液 ②c(H+)=c(OH-)的溶液 ③c(H+)=1×10-6 mol·L-1的溶液 ④c(H+)>c(OH-)的溶液
⑤0.1 mol·L-1的NH4Cl溶液 ⑥NaHCO3溶液
A.①③④⑤⑥ B.②④⑤⑥
C.⑤⑥ D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质的分类或归类不正确的是()
①混合物:碘酒、盐酸、牛奶、水银
②化合物:CaCl2、烧碱、硫酸铜晶体、HD
③电解质:明矾、醋酸、硫酸钡
④纯净物:干冰、冰水混合物、浓硫酸
⑤同位素: C、
C、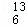 C、
C、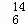 C.
C.
A. ①②③④ B. ①②④ C. ①③④⑤ D. ②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是()
A. 将Na2CO3固体加入新制的氯水中,有无色气泡(H+)
B. 向淀粉KI溶液中滴加新制氯水,溶液变蓝(Cl2)
C. 将AgNO3溶液滴加到新制氯水中,有白色沉淀产生(Cl﹣)
D. 新制氯水使红色布条褪色(HCl)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:KClO3+NH4NO2→KCl+NH4NO3
(1)指出以上反应中的氧化剂是KClO3,被氧化的元素是N;
(2)配平上述反应方程式并标明电子转移的方向和数目 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示对应化学反应的化学方程式或离子方程式正确的是
|
B.双氧水催化分解:H2O2 ===== H2 ↑+ O2↑
C.草酸与酸性高锰酸钾反应的离子方程式: H2C2O4+6H++MnO4-=Mn2-+4H2O+2CO2↑
D.FeCl3溶液中加入几滴KSCN : FeCl3+ 3KSCN  Fe(SCN)3↓+3KCl
Fe(SCN)3↓+3KCl
查看答案和解析>>
科目:高中化学 来源: 题型:
有七种物质:①甲烷、②苯、③聚乙烯、④聚异戊二烯、⑤2﹣丁炔、⑥环己烷、⑦环己烯,既能使酸性高锰酸钾溶液褪色,又能使溴水因反应而褪色的是( )
|
| A. | ③④⑤⑧ | B. | ④⑤⑦ | C. | ④⑤ | D. | ③④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
苯甲酸(C6H5COOH)和山梨酸(CH3—CH===CH—CH===CH—COOH)都是常用的食品防腐剂。下列物质中,只能与其中一种酸发生反应的是( )
A.Na B.溴水
C.CH3CH2OH D.NaOH溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com