
分析 E能连续被氧化生成羧酸,从E到HOOCCOOH,反应过程中碳原子个数不变,所以E为CH2OHCH2OH、F为OHCCHO,A光照发生反应生成B,且B比A相对分子质量大79,则A发生取代反应生成B,B发生消去反应生成C,C发生加成反应生成D,则A为烷烃、B为溴代烷、C是烯烃、D是二溴代烷,据此分析解答.
解答 解:E能连续被氧化生成羧酸,从E到HOOCCOOH,反应过程中碳原子个数不变,所以E为CH2OHCH2OH、F为OHCCHO,A光照发生反应生成B,且B比A相对分子质量大79,则A发生取代反应生成B,B发生消去反应生成C,C发生加成反应生成D,这一系列反应碳原子个数不变,所以A、B、C、D分别是CH3CH3、CH3CH2Br、CH2═CH2、CH2BrCH2Br,
故答案为:CH3CH3;CH3CH2Br;CH2═CH2;CH2BrCH2Br;CH2OHCH2OH;OHC-CHO.
点评 本题考查有机物推断,侧重考查学生分析推断能力,涉及烷烃、卤代烃、醇、醛、羧酸之间的转化,明确常见有机反应类型及其反应条件是解本题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 与钠反应① | B. | 在铜催化下加热①③ | ||
| C. | 在浓硫酸170°C条件下加热②③ | D. | 与HCl反应生成氯乙烷② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 在侯氏制碱工业中,向饱和氯化钠溶液中先通二氧化碳,后通氨气 | |
| B. | 在硫酸工业、合成氨工业、硝酸工业中,皆采用循环操作提高原料利用率 | |
| C. | 在氯碱工业,电解槽一般用铁网作电极 | |
| D. | 合成氨工业用天然气造气的方法中,与水蒸汽高温反应优于热分解法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 温度/℃ | 200℃ | 250℃ | 300℃ |
| 平衡常数/(mol•L-1)2 | K1 | K2 | 80 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
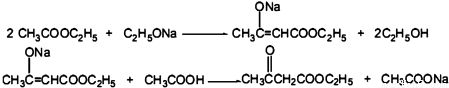

 CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com