
【题目】科学家开发出一种新型锂—氧电池,其能量密度极高,效率达90%以上。电池中添加碘化锂(LiI)和微量水,工作原理如图所示,总反应为:O2+4LiI+2H2O2I2+4LiOH

对于该电池的下列说法不正确的是( )
A.放电时负极上I- 被氧化
B.充电时Li+从阳极区移向阴极区
C.充电时阴极反应为LiOH+e-==Li+OH-
D.放电时正极反应为O2+2H2O+4Li++4e-==4LiOH
科目:高中化学 来源: 题型:
【题目】利用反应2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) ΔH=-746.8 kJ·mol-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是
2CO2(g)+N2(g) ΔH=-746.8 kJ·mol-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是
A.降低温度 B.升高温度同时充入N2
C.增大压强同时加催化剂 D.及时将CO2和N2从反应体系中移走
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 有机物分子中一定含有一个或多个碳原子
B. 有机物分子中的碳原子可以相互连接成链状或环状
C. 有机物分子中的碳原子可以与其它元素的原子连接
D. 分子中含有碳原子的化合物一定是有机化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学―选修2:化学与技术】以硫铁矿(主要成分为FeS2)为原料制取硫酸,其矿渣可用来炼铁。生产工艺示意图如下:
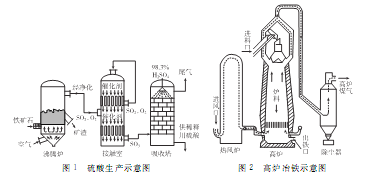
(1)配平煅烧硫铁矿的反应方程式:______FeS2+________O2→_____Fe2O3+______SO2。实际生产中向沸腾炉通入的空气量要大于锻烧硫铁矿所需空气量.其目的是____________________。接触室和热风炉中都装有热交换器,可用反应的余热将通入的气体加热,这样做的好处是_____________________。
(2)生产硫酸时,吸收塔中用98.3%的硫酸吸收而不用水吸收SO3的原因是______________。用含FeS280%的硫铁矿生产硫酸,如果煅烧时有5%的硫损失,SO2转变成SO3的转化率为80%,那么生产98%的浓硫酸3吨,则需要这种硫铁矿___________吨。
(3)CO还原Fe2O3的冶铁过程中,反应物、生成物和温度之间的关系如图所示.
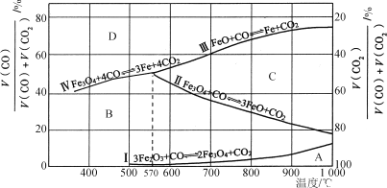
(图中Ⅰ、Ⅱ、Ⅲ、Ⅳ四条曲线是四个化学反应平衡时的气相组成对温度作图得到的;A、B、C、D四个区域分别是Fe2O3、Fe3O4、FeO、Fe稳定存在的区域)
①冶炼高炉产生的高炉煤气的主要成分有__________和剩余的CO。
②据图分析,下列说法正确的是________(填字母)。
a.温度低于570 ℃时,Fe2O3还原焙烧的产物中不含FeO
b.温度越高,Fe2O3还原焙烧得到的固体物质组成中Fe元素的质量分数越高
c.Fe2O3还原焙烧过程中及时除去CO2有利于提高Fe的产率
③800℃时,混合气体中CO2体积分数为40%时,Fe2O3用CO还原焙烧反应的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中,可以大量共存的离子组是
A. Fe3+、K+、S2-、Cl- B. Al3+、HCO3-、SO42-、Cl-
C. K+、NH4+、SiO32-、NO3- D. K+、Cl-、SO42-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中正确的是 ( )
A.蒸馏原理适用于分离互不相溶的液体混合物
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶支管口处
C.蒸馏操作时,冷凝管中冷却水应该是上口进下口出
D.蒸馏操作时,沸点高的物质先被蒸出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学们对SO2通入漂粉精溶液的反应进行实验探究:
操作 | 现象 |
取4 g 漂粉精固体,加入100 mL 水 | 部分固体溶解,溶液略有颜色 |
过滤,测漂粉精溶液的pH | pH 试纸先变蓝(约为12),后褪色 |
| 1.液面上方出现白雾; 2.稍后,出现浑浊,溶液变为黄绿色; 3.稍后,产生大量白色沉淀,黄绿色褪去 |
(1)Cl2和Ca(OH)2制取漂粉精的反应中氧化剂与还原剂的物质的量之比为__________。
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是____________。
(3)兴趣小组将A中产生的白雾引出导入硝酸酸化的AgNO3溶液中,有沉淀产生,据此判断白雾成分为HCl小液滴,该结论合理吗?________(填“合理”或“不合理”),并说明理由__________________。
(4)现象2中溶液变为黄绿色的原因是:随溶液酸性的增强,漂粉精的有效成分和Cl发生反应。该反应的离子方程式为______________。
(5)①将A瓶中混合物过滤、洗涤,得到沉淀X,X的成分是____________(填化学式);
②用离子方程式解释现象3中黄绿色褪去的原因____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com