


科目:高中化学 来源:2013届江苏省高二下学期期末考试化学选修试卷(解析版) 题型:选择题
下列关于微粒结构的描述正确的是
A.CS2为V形的极性分子
B.ClO3—的空间构型为平面三角形
C.SF6中有6对完全相同的成键电子对
D.SiF4和SO 32—的中心原子均为sp3杂化
查看答案和解析>>
科目:高中化学 来源:2010年广州市等四校联考高一第二学期期末考试化学试题 题型:选择题
下列关于微粒结构的描述,正确的是
A.氯化氢电子式:H׃Cl
B.O2―的结构示图:
C.CaCl2的电子式: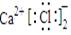 D.F原子结构示意:
D.F原子结构示意:
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
| A.CS2为V形的极性分子 |
| B.ClO3- 的空间构型为平面三角形 |
| C.SF6中有6对完全相同的成键电子对 |
| D.SiF4和SO32- 的中心原子均为sp3杂化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com