

分析 (1)从所加入物质能增大溶液离子浓度,并能保持污水的pH在5.0~6.0之间考虑;
(2)根据电极材料和离子的放电顺序考虑;
(3)二价铁离子具有还原性,能被氧气氧化到正三价,而溶液呈酸性,所以反应①和②的生成物反应得到Fe(OH)3沉淀的离子方程式为:4Fe2++10H2O+O2=4Fe(OH)3↓+8H+;
(4)燃料电池中,正极发生的反应是氧气得电子被还原的过程,负极发生的反应是燃料失电子被氧化的过程;电池是以熔融碳酸盐为电解质,可以循环利用的物质只有二氧化碳.
解答 解:(1)为了增强溶液的导电性,因此可选用易溶性强电解质溶液,排除A和B,考虑到题中要求电解时保持污水的pH在5.0~6.0之间,因此不能添加NaOH,BaSO4不溶,故答案为:C;
(2)电解时铁作阳极,因此主要发生Fe-2e-=Fe2+,同时也发生副反应,即溶液中的OH-失电子被氧化生成O2,故答案为:Fe-2e-=Fe2+;2H2O-4e-=4H++O2↑;
(3)二价铁离子具有还原性,能被氧气氧化到正三价,而溶液呈酸性,所以反应①和②的生成物反应得到Fe(OH)3沉淀的离子方程式为:4Fe2++10H2O+O2=4Fe(OH)3↓+8H+,故答案为:4Fe2++10H2O+O2=4Fe(OH)3↓+8H+;
(4)料电池中,正极反应一定是氧气得电子,该电池的电解质环境是熔融碳酸盐,所以正极反应为:O2+2CO2+4e-=2CO32-;负极反应是CH4失电子,该电池的电解质环境是熔融碳酸盐,所以负极反应为:CH4+4CO32--8e-=5CO2+2H2O;电池是以熔融碳酸盐为电解质,可以循环利用的物质只有二氧化碳;
故答案为:O2+2CO2+4e-=2CO32-;CO2.
点评 本题考查原电池和电解池的知识,较为综合,做题时注意利用守恒的思考去解答,同时注意电极反应式的书写.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源:2016-2017学年黑龙江大庆铁人中学高二上期中化学试卷(解析版) 题型:填空题
课题式研究性学习是培养学生创造性思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。
试回答下列问题:
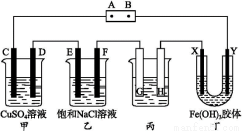
(1)电源A极的名称是 。
(2)甲装置中电解反应的总化学方程式: 。
(3)如果收集乙装置中产生的气体,两种气体的体积比是 。
(4)欲用丙装置给铜镀银,G应该是 (填“铜”或“银”),电镀液的主要成分是 (填化学式)。
(5)装置丁中的现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A2B | B. | AB2 | C. | AB3 | D. | A2B5 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 纯净的苯酚是粉红色的晶体 | |
| B. | 有特殊的气味 | |
| C. | 易溶于乙醇、乙醚等有机溶剂,不易溶于冷水 | |
| D. | 苯酚有毒,沾在皮肤上,可用浓NaOH溶液洗涤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HOCH2COOCH2CH3 | B. | CH3CH(OH)CH2COOH | C. | HOCH2CH2CH2COOH | D. | CH3CH2CH(OH)COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 铜是负极,铜片上有气泡产生 | |
| B. | 铜片是正极,该电极周围溶液pH不变 | |
| C. | 电子流从锌片经导线流向铜片 | |
| D. | 氢离子在锌片表面被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸钠固体 | B. | 硫酸铜固体 | C. | 硝酸钾溶液 | D. | 氯化钠溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com