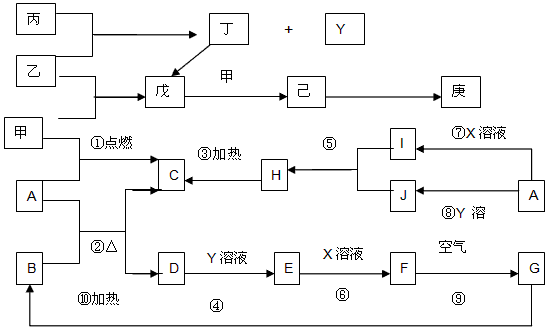
图甲中A-J均为中学化学中常见的物质,A、H是短周期元素组成的常见气体单质,B是日常生活常见金属,它们之间有如下转化关系(反应中生成的水及部分生成物已略去).请回答以下问题:
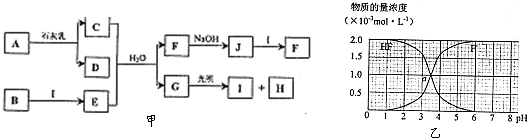
(1)D的电子式是
,G的结构式是
;
(2)C的水溶液显
(填“酸性”、“碱性”或“中性”),其原因是
(用离子方程式表示);
(3)写出J+I→F的离子方程式:
;
(4)在298K,100kPa时,在1L水中可溶解0.09mol A,实验测得溶于水的A约有
与水反应,请估算该离子反应的平衡常数K=
;(忽略溶液体积变化)
(5)25℃时,2.0×10
-3mol?L
-1HF溶液中,调节溶液pH(忽略溶液体积变化)得到(HF)、c(F
-)与溶液pH的变化关系如图乙.若将4.0×10
-3mol?L
-1HF溶液与4.0×10
-3mol?L
-1CaCl
2溶液等体积混合,调节混合液pH=4(忽略调节时混合液体积的变化),通过列式计算说明是否有CaF
2沉淀析出.[已知K
sp(CaF
2):1.5×10
-10].


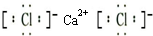 ,G是次氯酸,次氯酸分子的中心原子是O原子,次氯酸分子的结构式是H-O-Cl,
,G是次氯酸,次氯酸分子的中心原子是O原子,次氯酸分子的结构式是H-O-Cl,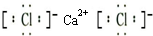 ;H-O-Cl;
;H-O-Cl;