
铁氧体(Fe3O4)法是处理含铬废水的常用方法.其原理是:用FeSO4把废水中Cr2O72-还原为Cr3+,并通过调节废水的pH,使生成物组成符合类似于铁氧体(Fe3O4或Fe2O3·FeO)的复合氧化物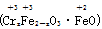 。 处理含1 mol Cr2O72-废水至少需要加入a mol FeSO4·7H2O。下列结论正确的是
。 处理含1 mol Cr2O72-废水至少需要加入a mol FeSO4·7H2O。下列结论正确的是
A.x=1,a=5 B.x=0.5,a=8
C.x=2,a=10 D.x=0.5,a=10
科目:高中化学 来源:2014-2015学年吉林省高一下期末化学试卷(解析版) 题型:选择题
下列叙述中正确的是
A.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数
B.除短周期外,其他周期均有18种元 素
素
C.副族元素中没有非金属元素
D.碱金属元素是指IA族的所有元素
查看答案和解析>>
科目:高中化学 来源:2016届福建省福州市高三上学期第二次质量检测考试化学试卷(解析版) 题型:选择题
下列有关性质的比较,不能用元素周期律解释的是
A.酸性:H2SO4>H3PO4 B.非金属性:Cl>Br
C.碱性:NaOH>Mg(OH)2 D.热稳定性:Na2CO3>NaHCO3
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上学期第一次月考化学试卷(解析版) 题型:实验题
(18分)1000mL某待测液中除含有0.2 mol·L-1的Na+外,还可能含有下列离子中的一种或多种:
阳离子 | K+、NH4+、Fe3+、Ba2+ |
阴离子 | Cl-、Br-、CO32-、HCO3-、SO32-、SO42- |
现进行如下实验操作(所加试剂均过量):
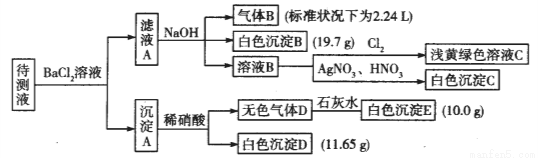
(1)写出生成白色沉淀B的离子方程式:_______________。
(2)待测液中肯定不存在的阳离子是_____________。
(3)若无色气体D是单一气体:
①将阴离子的物质的量浓度填入下表中(一定不存在的填“0”,不能确定的填“?”):
阴离子 | Cl- | Br- | CO32- | HCO3- | SO32- | SO42- |
浓度/ mol·L-1 |
②判断原溶液中K+是否存在,若存在,求其物质的量浓度的最小值,若不存在,请说明理由:__________。
(4)若无色气体D是混合气体:
①待测液中一定含有的阴离子是__________。
②沉淀A中能还原稀硝酸的成分是________________(写化学式)。
查看答案和解析>>
科目:高中化学 来源:2016届河北省冀州市高三复习班上第一次月考化学试卷A(解析版) 题型:实验题
(10分)某科研小组探究工业废Cu粉(杂质含有SiO2、Al2O3、Fe2O3中的一种或几种)的组成并制备少量CuSO4·5H2O,实现废物综合利用,实验过程如下:
过程Ⅰ:
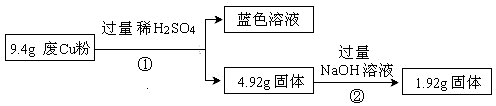
(1)废Cu粉中一定含有的杂质是 (填化学式)。
(2)写出过程②发生反应的离子方程式: 。
过程Ⅱ:
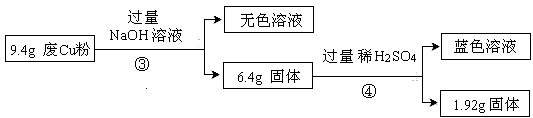
(3)综合过程Ⅰ、II,计算废Cu粉中各成分的质量之比是 (化为最简整数比)
过程Ⅲ:已知25℃时:
电解质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
溶度积(Ksp) | 2.2×10-20 | 8.0×10-16 | 4.0×10-38 |
开始沉淀时的pH | 5.4 | 6.5 | 3.5 |
完全沉淀时的pH | 6.4 | 9.6 | 4.0 |
(4)在Ⅱ中所得蓝色溶液中加入一定量的H2O2 溶液,调节溶液的pH范围为 ,然后过滤、结晶,可得CuSO4·5H2O。
(5)下列与 Ⅲ方案 相关的叙述中,正确的是 (填字母)。
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+ 氧化为Fe3+ 的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.调节溶液pH选择的试剂可以是氢氧化铜或氧化铜
D.在pH>4的溶液中Fe3+一定不能大量存在
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期二调化学试卷(解析版) 题型:选择题
如图所示的实验,发现烧杯中酸性KMn04溶液褪色。若将烧杯中的溶液换成含有少量KSCN
的FeS04溶液,溶液呈血红色。判断下列说法中不正确的是
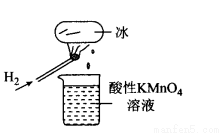
A.该条件下H2燃烧生成了既具有氧化性又具有还原性的物质
B.该条件下H2燃烧的产物中可能含有一定量的H202
C.将烧杯中溶液换成KI淀粉溶液也能验证生成物具有还原性
D.酸性FeSO4溶液中加入双氧水的离子反应为:2Fe2++H2O2+2H+=2Fe3+ +2H20
查看答案和解析>>
科目:高中化学 来源:2016届安徽省合肥市高三上第二次段考化学试卷(解析版) 题型:实验题
(11分)硫酸锰可作为饲料添加剂用于增肥,也可用于某些化学反应的催化剂,易溶于水,不溶于乙醇。工业上常用软锰矿(主要成分为MnO2,含有MgSO4等杂质)制备硫酸锰,其简化流程如下:
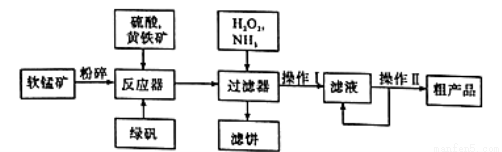
(1)为了加快软锰矿与硫酸、黄铁矿反应的速率,工业上除采用粉碎软锰矿的方法,还可以用哪些方法 (写两种)。
(2)流程中黄铁矿(主要含FeS2)和FeSO4的作用都是作还原剂,请写出FeSO4与软锰矿反应的离子方程式 。
(3)双氧水和氨水的作用分别是 .
(4)操作II包括 、 、 、洗涤、干燥,可制得MnSO4·H2 O粗产品.洗涤中最好选用 ’
A.稀硫酸 B.水 C.乙醇 D.浓硫酸
查看答案和解析>>
科目:高中化学 来源:2016届河南省洛阳市高三上学期周练化学试卷(解析版) 题型:选择题
把一块镁铝合金投入到1mol/L 盐酸里,待合金完全溶解后,往溶液里加入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如下图A所示。下列说法中不正确的是
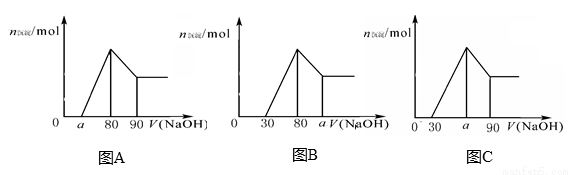
A.a的取值范围为0≤ a<50
B.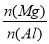 的最大值为2.5
的最大值为2.5
C.若将关系图改为B图时,则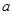 的取值范围为80<a<90
的取值范围为80<a<90
D.若将关系图改为C图时,则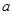 的取值范围为75<a<90
的取值范围为75<a<90
查看答案和解析>>
科目:高中化学 来源:2016届河南省高三上学期开学考试化学试卷(解析版) 题型:选择题
羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡: CO(g)+H2S(g) COS(g)+H2(g) K=0.1反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是
COS(g)+H2(g) K=0.1反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是
A.升高温度,H2S浓度增加,表明该反应是吸热反应
B.通入CO后,正反应速率逐渐增大
C.反应前H2S物质的量为7mol
D.CO的平衡转化率为80%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com