
内锌矿的主要成分为ZnS,含有杂质PbS、CuS、FeS、SiO2等,以闪锌矿制备氯化锌的流程如图所示。
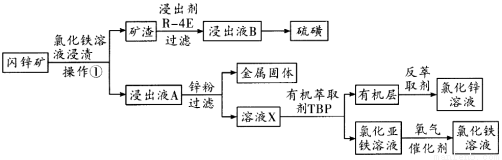
请回答下列问题:
(1)配制氯化铁浸渍液时要求pH为0.8~1之间,pH太高则 ,pH太低,浸渍矿石会产生有害气体 ,操作①是 。由氯化锌溶液制备氯化锌晶体的方法是 。
(2)高沸点溶剂R—4E几乎不溶于水,120℃时硫在R—4E里的溶解度为365g,室温时溶解度为35.9g,从浸出液B提取硫的方法是 。硫是工业制备硫酸的原料,现有1吨矿石,硫的总含量为24%,最多制备浓度98%的硫酸 吨。
(3)氯化铁与硫化锌发生反应: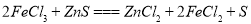 ,则氯化铁与FeS反应的方程式为 。
,则氯化铁与FeS反应的方程式为 。
(4)溶液X的成分的化学式为 ,该流程中循环使用的物质是 。
(5)由氯化亚铁溶液制备氯化铁溶液,可以用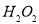 、
、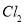 ,但生产成本高。酸性条件下,使用催化剂在50℃左右通入氧气转化的成本极低,反应的离子方程式为 。
,但生产成本高。酸性条件下,使用催化剂在50℃左右通入氧气转化的成本极低,反应的离子方程式为 。
科目:高中化学 来源:2017届广东省高三上学期摸底考试理综化学试卷(解析版) 题型:选择题
选项 | 实验操作 | 实验现象 | 结论 |
A | 将FeCl3饱和溶液滴入一定量的沸水中得红褐色透明液体,用激光笔照射 | 有丁达尔效应 | 红褐色液体为胶体 |
B | 将FeSO4高温强热,得红棕色固体,产生的气体通入足量BaCl2溶液 | 产生白色沉淀 | 白色沉淀为BaSO4和BaSO3 |
C | 将气体X分别通入品红溶液和酸性高锰酸钾溶液 | 两溶液均褪色 | X可能是乙烯 |
D | 向溶液Y中滴加硝酸,再滴加BaCl2溶液 | 有白色沉淀生成 | Y中一定含有SO42- |
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上学期开学考试化学试卷(解析版) 题型:选择题
A元素的阳离子与B元素的阴离子具有相同的电子层结构,下列有关两元素的叙述中正确的是( )
①原子半径:A <B ②离子半径:A>B ③原子序数:A>B
④第一电离能:A>B ⑤A的正价与B的负价的绝对值相等 ⑥电负性:A<B
A. ①② B. ③⑥ C. ③⑤ D. ③④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上适应性考试(一)理综化学试卷(解析版) 题型:选择题
a、b、c、d四种元素在周期表中的位置如下图,则下列说法正确的是
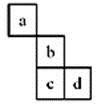
A. 若b的最高价氧化物对应水化物为H2bO4,则a的氢化物的化学式为aH3
B. 若b的单质可作半导体材料,则c的单质不可能为半导体材料
C. 若b的单质与H2易化合,则c的单质与H2更易化合
D. a与b之间容易形成离子化合物
查看答案和解析>>
科目:高中化学 来源:2017届安徽省六安市高三上第一次月考化学试卷(解析版) 题型:实验题
(14分)硼位于ⅢA族,三卤化硼是物质结构化学的研究热点,也是重要的化工原料。三氯化硼(BCl3)可用于制取乙硼烷(B2H6),也可作有机合成的催化剂。
【查阅资料】
①BCl3的熔点为-107.3 ℃,沸点为12.5 ℃;
②2B+6HCl 2BCl3↑+3H2↑;
2BCl3↑+3H2↑;
③硼与铝的性质相似,也能与氢氧化钠溶液反应。
【设计实验】 某同学设计如图所示装置制备三氯化硼:

请回答下列问题:
(1)常温下,高锰酸钾固体粉末与浓盐酸发生的反应可替代A装置中的反应,两个反应的产物中锰的价态相同。写出高锰酸钾固体粉末与浓盐酸反应的离子方程式:______________。
(2)E装置的作用是________________。
(3)写出D装置中发生反应的化学方程式:__________________;实验中可以用一个盛装________(填试剂名称)的干燥管代替F+G装置,使实验更简便。
(4)三氯化硼遇水剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式________________。
(5)为了顺利完成实验,正确的操作是__________(填序号)。
①先点燃A处酒精灯,后点燃D处酒精灯
②先点燃D处酒精灯,后点燃A处酒精灯
③同时点燃A、D处酒精灯
(6)请你设计一个简易实验,验证制得的产品中是否含有硼粉:____________________
查看答案和解析>>
科目:高中化学 来源:2017届安徽省六安市高三上第一次月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数值。下列有关叙述正确的是
A.在O2参与的反应中,1 mol O2作氧化剂时得到的电子数一定是4NA
B.50mL18.4 mol/L浓硫酸与足量铜加热反应,生成SO2分子的数目为0.46NA
C.1 molFe溶于过量硝酸,电子转移数为2NA
D.78g Na2O2晶体中含有的离子数目为3NA
查看答案和解析>>
科目:高中化学 来源:2017届河南省灵宝市高三上学期9月月考化学试卷(解析版) 题型:实验题
(1)实验室用锌片和稀硫酸反应制取氢气,并验证氢气的还原性及回收硫酸锌晶体。
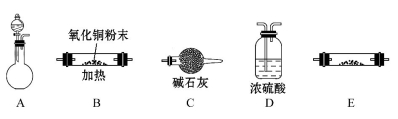
①各仪器的连接顺序为________________,装置C的作用是_________________。
②锌与硫酸反应制取氢气后的剩余废液中,常含有少量剩余的硫酸,欲除去多余的硫酸并回收硫酸锌晶体,请从BaCl2溶液、锌粉、NaOH溶液三种试剂中选用一种试剂除杂并简述回收硫酸锌晶体的实验过程______________________。
(2)工业上由锌白矿(主要成分是ZnO,还含有Fe2O3、CuO、SiO2等杂质)制备ZnSO4·7H2O的流程如下。
已知:常温下,溶液中的Fe3+、Zn2+、Fe2+以氢氧化物形式完全沉淀的pH分别为3.7、6.5、9.7。
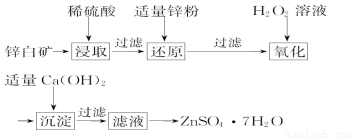
①为了提高酸浸效率,可以采取的措施有_____________、 (写出两条即可)。
②氧化过程中H2O2发生反应的离子方程式为___________________________。
③由滤液得到ZnSO4·7H2O的操作依次为__________、___________、过滤、洗涤、干燥。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com