
 ⑥+
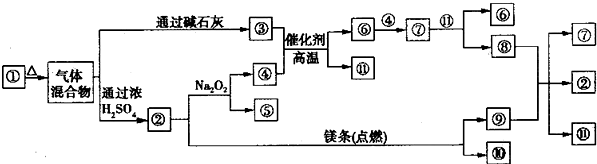
⑥+ ?,知④为O2则⑤为Na2CO3,③为NH3,其余依次推出:①为(NH4)2CO3或NH4HCO3,⑥为NO,⑦为NO2,⑧为HNO3,⑨为C,⑩为MgO,
?,知④为O2则⑤为Na2CO3,③为NH3,其余依次推出:①为(NH4)2CO3或NH4HCO3,⑥为NO,⑦为NO2,⑧为HNO3,⑨为C,⑩为MgO, 为H2O,
为H2O, 4NO2↑+CO2↑+2H2O,
4NO2↑+CO2↑+2H2O, 4NO2↑+CO2↑+2H2O;
4NO2↑+CO2↑+2H2O; C+2MgO,故答案为:CO2+2Mg
C+2MgO,故答案为:CO2+2Mg C+2MgO.
C+2MgO. ⑥+
⑥+ ?,知④为O2则⑤为Na2CO3,③为NH3,其余依次推出:①为(NH4)2CO3或NH4HCO3,⑥为NO,⑦为NO2,⑧为HNO3,⑨为C,⑩为MgO,
?,知④为O2则⑤为Na2CO3,③为NH3,其余依次推出:①为(NH4)2CO3或NH4HCO3,⑥为NO,⑦为NO2,⑧为HNO3,⑨为C,⑩为MgO, 为H2O.结合对应物质的性质解答该题.
为H2O.结合对应物质的性质解答该题.

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com