
莽草酸是合成达菲的主要原料,其结构简式如图,下列说法正确的是:( )

A. 分子式为C7H8O5 B.能使溴的四氯化碳溶液褪色
C.只能发生加成反应和取代反应 D.分子中含有2种官能团
科目:高中化学 来源:2016-2017学年吉林省长春市五县高二上期末化学试卷(解析版) 题型:选择题
某新型蓄电池放电、充电时的反应为Fe+Ni2O3+3H2O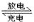 Fe(OH)2+2Ni(OH)2。下列推断中不正确的是( )
Fe(OH)2+2Ni(OH)2。下列推断中不正确的是( )
A.充电时,Ni(OH)2为阳极
B.放电时,Fe为正极,Ni2O3为负极
C.该新型蓄电池的电解质溶液呈碱性
D.充电时,阴极反应式为Fe(OH)2+2e-=Fe+2OH-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林省两省六校高二上期中化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.在水溶液里能够电离出阴、阳离子的化合物是强电解质.
B.强电解质的水溶液一定能导电;非电解质的水溶液一定不导电.
C.强电解质的水溶液的导电性一定比弱电解质强.
D.相同条件下,pH相同的盐酸和醋酸的导电性相同。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林省两省六校高二上期中化学试卷(解析版) 题型:选择题
在醋酸的下列性质中,可以证明它是弱电解质的是
A.1mol/L的醋酸溶液中H+浓度约为10-3mol/L
B.醋酸能与水以任意比互溶
C.10mL 1mol/L的醋酸恰好与10mL 1mol/L NaOH溶液完全反应
D.醋酸的导电性比强酸溶液弱
查看答案和解析>>
科目:高中化学 来源:2017届广东省惠州市高三上第三次调研化学试卷(解析版) 题型:选择题
下列有关NaClO和NaCl混合溶液的叙述正确的是 ( )
A.该溶液中,H+、NH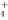 、SO
、SO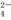 、I-可以大量共存
、I-可以大量共存
B.该溶液中,Ag+、K+、NO 、NH
、NH 可以大量共存
可以大量共存
C.该溶液中, Fe2+、Fe3+、Cl-、NO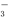 可以大量共存
可以大量共存
D.向该溶液中加入浓盐酸,每产生1 molCl2,转移电子约为6.02×1023个
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三上第二次段考化学试卷(解析版) 题型:实验题
晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:
①高温下用炭还原二氧化硅制得粗硅;
②粗硅与干燥HCl气体反应制得SiHCl3:Si+3HCl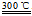 SiHCl3+H2;
SiHCl3+H2;
③SiHCl3与过量H2在1000~1100 ℃反应制得纯硅。
已知:SiHCl3能与H2O强烈反应,在空气中易自燃。
请回答下列问题:
(1)第①步制备粗硅的化学方程式为_____________________。
(2)用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):
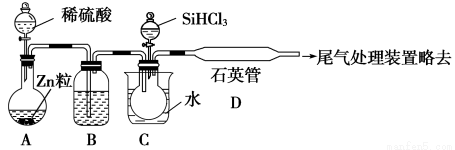
①装置B中的试剂是________。装置C中的烧瓶需要加热,其目的是_________________。
②反应一段时间后,装置D中观察到的现象是________________,装置D中发生反应的化学方程式为__________________________。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及__________________________。
④SiHCl3的电子式为________,SiHCl3与H2O反应的化学方程式为:_________________。
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三上第二次段考化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值。下列说法正确的是( )
A.2.0g D2O中含有的质子数、中子数均为NA
B.标准状况下,22.4 L CCl4含有NA个CCl4分子
C.1 mol Fe2+与足量的H2O2溶液反应,转移2NA个电子
D.一定条件下1 mol N2和3 mol H2充分反应后分子总数为2NA
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上联考二化学卷(解析版) 题型:实验题
Ⅰ.某化学兴趣小组用以下装置探究SO2的某些化学性质。
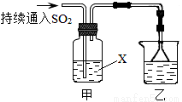
(1)装置乙的作用是 。
(2)若X为品红溶液,观察到溶液褪色,说明SO2具有 (填序号,下同);
若X为Na2S溶液,观察到溶液中出现淡黄色浑浊,说明SO2具有 ;
a.氧化性 b.还原性 c.漂白性
(3)若试剂X为Ca(ClO)2溶液,可观察到白色沉淀生成,完成该过程的离子方程式:
 Ca2++
Ca2++ ClO-+
ClO-+ SO2+
SO2+ H2O=
H2O= CaSO4↓+
CaSO4↓+ Cl-+
Cl-+ SO42-+
SO42-+ 。
。
Ⅱ.某兴趣小组为探究沉淀溶解平衡的原理并测定某温度下PbI2溶度积常数,设计如下实验。
i.取100mL蒸馏水,加入过量的PbI2固体(黄色),搅拌,静置,过滤到洁净的烧杯中,得到滤液。
(4)搅拌的目的是 。
(5)取少量滤液于试管中,向其中滴加几滴0.1 mol·L-1KI溶液,观察到的现象是 。
ii.准确量取10.00mL滤液,与离子交换树脂(RH)发生反应:2RH + Pb2+= R2Pb + 2H+,交换完成后,流出溶液用滴定法测得n(H+)=3.000×10-5 mol。
(6)在此实验温度下,PbI2的溶度积常数Ksp= 。若步骤i盛装滤液的烧杯中有少量水,Ksp测定结果将会 (填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源:2017届广东省肇庆市高三上学期二模化学试卷(解析版) 题型:选择题
一种二次电池如图所示,该电池的电解质为强碱溶液,下列说法中正确的是( )
A.充电时阴极发生氧化反应
B.充电时将碳电极与电源的正极相连
C.放电时碳电极反应为原电池的负极
D.放电时镍电极反应为Ni(OH)2-e-+OH-=NiO(OH)+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com