
(每空2分,共18分)现有A、B、C、D、E五种物质,并存在如下转化关系.其中E为黑色粉末,在下图转化中均作催化剂

(1)B的化学式
(2)利用下图所示的实验装置进行C与水的反应,回答下列有关同题:

① 固体C与水反应生成D的化学方程式为: .
② 检验导管出口气体的方法为: .
③烧杯中的现象为: .
(3)在加热条件下,某无氧酸(含有A中的一种元素)的浓溶液与E反应,生成单质气体X.为检验X的性质,设计如下图所示实验装置:

①实验过程中,观察到装置Ⅲ中的品红试纸的红色褪去,并未观察到“无明显变化”这一预期现象.为了达到这一预期现象,你认为应该如何改进?
。
②实验结束后,装置Ⅳ中可观察到现象是 ,若滴加两滴胶头滴管中的试剂,观察到溶液呈血红色,有关的离子方程式为:
, 。
③X是一种重要的化工原料,用化学方程式表示X在化工生产上的一项用途:
。
(每空2分,共18分)(1)H2O2
(2) ①2Na2O2 + 2H2O = 4NaOH + O2↑②用带火星的木条靠近导管出口,观察木条是否复燃。
(或“用排水集气法收集一试管气体,用带火星的木条伸入试管中,观察木条是否复燃。”)
③出现浑浊(或“产生白色沉淀”)(3) ①在装置II、Ⅲ之间加入一个盛有浓硫酸的洗气瓶;②溶液由浅绿色变为黄色2Fe2+ + Cl2 = 2Fe3+ + 2Cl- 、Fe3+ + 3SCN- = Fe(SCN)3 (其他合理的写法均可)
③H2+Cl2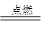 2HCl(写“光照”不得分)或2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O或CH2=CH2+Cl2CH2Cl—CH2Cl (其他合理答案均可)
2HCl(写“光照”不得分)或2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O或CH2=CH2+Cl2CH2Cl—CH2Cl (其他合理答案均可)
【解析】C是淡黄色固体,则C是过氧化钠,所以D是氧气。因此A是氯酸钾,E是二氧化锰,B是双氧水。
(1)双氧水的化学式为H2O2。
(2)①过氧化钠和水反应的方程式为2Na2O2 + 2H2O = 4NaOH + O2↑。
②检验氧气可以用带火星的木条靠近导管出口,观察木条是否复燃。
③过氧化钠和水反应是放热反应,溶液中OH-浓度增大,且氢氧化钙的溶解度降低,所以会析出晶体、
(3)①C是浓盐酸和二氧化锰反应生成氯气。由于起漂白作用的是次氯酸,所以要观察到“无明显变化”这一预期现象,需要除去氯气中混有的水蒸气,因此在装置II、Ⅲ之间加入一个盛有浓硫酸的洗气瓶。
②氯气具有氧化性,能氧化硫酸亚铁,生成硫酸铁,所以溶液由浅绿色变为黄色。方程式为2Fe2+ + Cl2 = 2Fe3+ + 2Cl-。铁离子没和KSCN溶液反应,用来检验铁离子,方程式为Fe3+ + 3SCN- = Fe(SCN)3。
③氯气可以用来制取盐酸、漂白粉等。


科目:高中化学 来源:2012-2013学年山东省德州市重点中学高二10月月考化学试卷(带解析) 题型:填空题
(每空2分,共18分)电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为 。在X极附近观察到的实验现象是 。
②Y电极上的电极反应式为 。检验该电极反应产物的方法是 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4 溶液,则:
①X电极的材料是 ,电极反应式为 。
②Y电极的材料是 ,电极反应式为 。
(说明:杂质发生的电极反应不必写出)
电解一段时间后,CuSO4溶液的浓度将 (填“变大”、“变小”或“不变”)
查看答案和解析>>
科目:高中化学 来源:2013届山东冠县武训高中高二下学期第三次考试化学试卷(解析版) 题型:实验题
(每空2分,共18分)
(一)实验室用下图装置制取少量溴苯,试填写下列空白。

(1)在烧瓶a中装的试剂是 。
(2)长直导管b的作用: 。
(3)请你分析导管c的下口可否浸没于液面中? (填“可”或 “否”)。
(4)反应完毕后,向锥形瓶d中滴加AgNO3溶液,有关反应的离子方程式: 。
(二)某课外活动小组利用下图装置进行乙醇的催化氧化实验并制取乙醛,图中铁架台等装置已略去,粗黑线表示乳胶管。请填写下列空白:

(1)甲装置常常浸在70~80℃的水浴中,目的是 。
(2)实验时,先加热玻璃管乙中的镀银铜丝,约1分钟后鼓入空气,此时铜丝即呈红热状态。若把酒精灯撤走,控制一定的鼓气速度,铜丝能长时间保持红热直到实验结束。
乙醇的催化氧化反应是________反应(填“放热”或“吸热”),
该反应的化学方程式为 。
(3)若试管丁中用水吸收产物,则要在导管乙、丙之间接上戊装置,其连接方法是
(填戊装置中导管代号):乙接 、_______接丙;
若产物不用水吸收而是直接冷却,应将试管丁浸在 _____ 中。
查看答案和解析>>
科目:高中化学 来源:2011-2012年山东聊城莘县实验高中高二第三次模块测试化学试卷(解析版) 题型:实验题
(每空2分,共18分)
(一)实验室用下图装置制取少量溴苯,试填写下列空白。
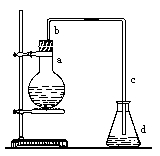
(1)在烧瓶a中装的试剂是 。
(2)长直导管b的作用: 。
(3)请你分析导管c的下口可否浸没于液面中? (填“可”或 “否”)
(4)反应完毕后,向锥形瓶d中滴加AgNO3溶液,有关反应的离子方程式: 。
(二)某课外活动小组利用下图装置进行乙醇的催化氧化实验并制取乙醛,图中铁架台等装置已略去,粗黑线表示乳胶管。请填写下列空白:
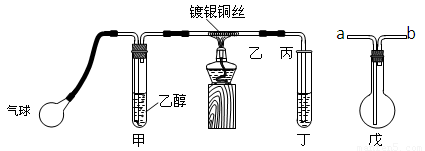
(1)甲装置常常浸在70~80℃的水浴中,目的是
(2)实验时,先加热玻璃管乙中的镀银铜丝,约1分钟后鼓入空气,此时铜丝即呈红热状态。若把酒精灯撤走,控制一定的鼓气速度,铜丝能长时间保持红热直到实验结束。
乙醇的催化氧化反应是________反应(填“放热”或“吸热”),
该反应的化学方程式为 。
(3)若试管丁中用水吸收产物,则要在导管乙、丙之间接上戊装置,其连接方法是
(填戊装置中导管代号):乙接 、_______接丙;
若产物不用水吸收而是直接冷却,应将试管丁浸在 _____ 中。
查看答案和解析>>
科目:高中化学 来源:2011-2012年河北省高二上学期9月份月考化学(理)试卷 题型:填空题
(每空2分,共18分)在实验室中做如下实验:一定条件下,在容积为2.0L的恒容密闭容器中,发生如下反应: 2A(g)+B(g)2C(g);△H =QkJ/mol
(1)若A、B起始物质的量均为零,通入C的物质的量(mol)随反应时间(min)的变化情况如下表:
|
序号 |
|
0 |
10 |
20 |
30 |
40 |
50 |
60 |
|
1 |
8 0 0 ℃ |
1.0 |
0.80 |
0.67 |
0.57 |
0.50 |
0.50 |
0.50 |
|
2 |
8 0 0 ℃ |
n2 |
0.60 |
0.50 |
0.50 |
0.50 |
0.50 |
0.50 |
|
3 |
8 0 0 ℃ |
n3 |
0.92 |
0.75 |
0.63 |
0.60 |
0.60 |
0.60 |
|
4 |
7 3 0 ℃ |
1.0 |
0.90 |
0.80 |
0.75 |
0.70 |
0.65 |
0.65 |
根据上表数据,完成下列填空:
①在实验1中反应在10至20min内反应的平均速率Vc= mol/(L·min);实验2中采取的措施是 ;实验3中n3 1.0 mol(填“>、=、<”)。
②比较实验4和实验1,可推测该反应中Q_ 0(填“>、=、<”),理由是_
(2)在另一反应过程中A(g)、B(g)、C(g)物质的量变化如右图所示,根据图中所示判断下列说法正确的__ __。

a.10~15 min可能是升高了温度
b.10~15 min可能是加入了催化剂
c.20 min时可能是缩小了容器体积
d.20 min时可能是增加了B的量
(3)一定条件下,向上述容器中通入5molA (g)和3molB(g),此时容器的压强为P(始)。
反应进行并达到平衡后,测得容器内气体压强为P(始)的 。若相同条件下,向上述
容器中分别通入a molA(g)、b molB(g)、c molC(g),欲使达到新平衡时容器内气体压
强仍为P(始)的 。
①a、b、c必须满足的关系是 , 。
(一个用a、c表示,另一个用b、c表示)
②欲使起始时反应表现为向正反应方向进行,则a的取值范围是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com