
| A、HB-的水解的离子方程式:HB-+H2O?H3O++B2- |
| B、溶液不含有H2B |
| C、溶液中:c(Na+)<c(HB-) |
| D、溶液中:c(OH-)>c(H+) |


 全能练考卷系列答案
全能练考卷系列答案科目:高中化学 来源: 题型:
| A、胶体都是胶状物质 | ||||
| B、溶液呈电中性,胶体带电荷 | ||||
| C、医疗上血液透析利用的是蛋白质、血细胞的微粒直径大于毒性物质的微粒直径的原理 | ||||
D、制备Fe(OH)3胶体的离子方程式为:Fe3++3H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
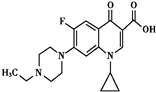 2012年4月18日沈阳和平区查获“毒豆芽”,其中添加一种动物用药恩诺沙星,其分子结构如图所示,下列有关恩诺沙星的说法中不正确的是( )
2012年4月18日沈阳和平区查获“毒豆芽”,其中添加一种动物用药恩诺沙星,其分子结构如图所示,下列有关恩诺沙星的说法中不正确的是( )| A、本品不溶于水,微溶于甲醇,可溶于酸和碱 |
| B、分子式为C19H22FN3O3 |
| C、该物质的一氯代物共有9种 |
| D、该物质能发生酯化、加成、氧化、硝化、缩聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C2H6 |
| B、C2H4 |
| C、C3H8 |
| D、C6H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素的非金属性依次增强 |
| B、元素的第一电离能依次增大 |
| C、最高价氧化物对应水化物的酸性依次减弱 |
| D、元素的原子半径依次减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com