
| A.该灰黑色粉末用作抗氧化剂 |
| B.小纸袋中的粉末是Fe2O3 |
| C.小纸袋中可能装有活性铁粉 |
| D.该灰黑色粉末不可食用 |
科目:高中化学 来源:不详 题型:单选题
| A.8.8 g | B.9.2g | C.8 g | D.16 g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
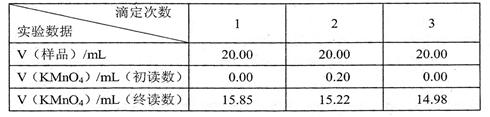
 [实验记录]
[实验记录] 2)本实验所用的KMnO4标准溶液的物质的量浓度为
2)本实验所用的KMnO4标准溶液的物质的量浓度为  。
。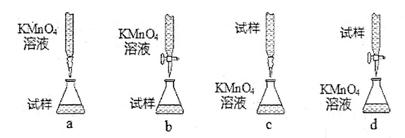
 洗一下,再继续滴定至终点,则所测得的补血剂中铁元素的含量 (偏大、偏小、无影响)。
洗一下,再继续滴定至终点,则所测得的补血剂中铁元素的含量 (偏大、偏小、无影响)。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
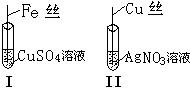
 是
是  ;
; ;
;查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Cu、Fe3+ | B.Fe2+、Fe3+ |
| C.Cu、Cu2+、Fe | D.Cu、Fe2+、Fe |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 白的副产品绿矾制备还原铁粉的工业流程如下:
白的副产品绿矾制备还原铁粉的工业流程如下: 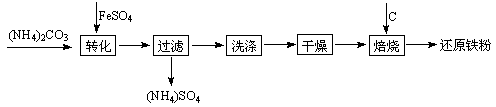
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com