
【题目】对于某反应X+3Y=2E+2F在甲、乙、丙、丁四种不同条件下。分别测得反应速率为甲:Vx=0.3mol·L-1·min-1;乙:VY=1.2mol·L-1·min-1;丙:VE=0.8mol·L-1·min-1;丁:VF=0.9mol·L-1·min-1,则反应最快的是 ( )
A.甲 B.乙 C.丙 D.丁
科目:高中化学 来源: 题型:
【题目】氨气在纯氧中燃烧(如图所示),生成化学性质稳定的气体X和水。下列说法正确的是
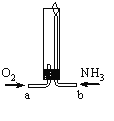
A.气体X的分子式为NO
B.N2、N4为元素N的两种同素异形体
C.该反应条件下,氨气的还原性小于水
D.两种气体通入的先后顺序是NH3、O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NaCl、CO2、NH3为原料发生反应,制得NaHCO3和NH4Cl是“侯氏制碱法”的重要步骤。相关物质的溶解度曲线如图所示。下列说法不正确的是
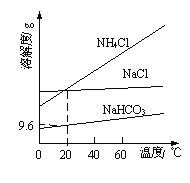
A.将NaHCO3加热分解可得纯碱
B.常温下碳酸氢钠的溶解度大于碳酸钠
C.采用蒸发结晶从溶液中分离出NaHCO3
D.20℃时,NaHCO3饱和溶液的物质的量浓度约为1.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列现象或事实可用同一原理解释的是
A.浓硫酸和浓盐酸长期暴露在空气中浓度降低 B.次氯酸和双氧水使品红试液褪色
C.氯水和水玻璃长期暴露在空气中变质 D.苯和乙烯使溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解CuCl2·2H2O制备CuCl,并进行相关探究。
【资料查阅】
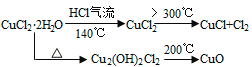
【实验探究】该小组用下图所示装置进行实验(夹持仪器略)。
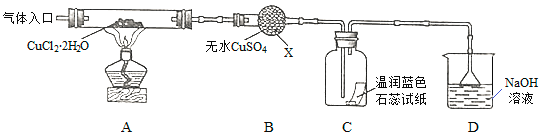
请回答下列问题:
(1)仪器X的名称是__________。
(2)实验操作的先后顺序是a→______→c(填操作的编号)
a.检查装置的气密性后加入药品
b.熄灭酒精灯,冷却
c.在“气体入口”处干燥HCl
d.点燃酒精灯,加热
e.停止通入HCl,然后通入N2
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是_______。
(4)装置D中发生的氧化还原反应的离子方程式是________________。
(5)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息分析:
①若杂质是CuCl2,则产生的原因是________________。
②若杂质是CuO,则产生的原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟氧酸是较新颖的氧化剂,应用性极强,可用被氮气稀释的氟气在细冰上缓慢通过制得:F2+H2O=HOF+HF.该反应中水的作用与下列反应中水的作用相同的是
A.钠与水反应制氢气
B.过氧化钠与水反应制氧气
C.氯气与水反应制次氯酸
D.氟单质与水反应制氧气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有学生在实验室中向盛有10mL饱和氯化铁溶液的试管里投入足量铝片,观察到如下现象:
①黄色溶液很快变成红褐色,过一会儿溶液中有红褐色沉淀生成。
②铝片表面立刻有少量黑色物质析出,黑色物质能被磁铁吸起。
③混合液温度升高甚至发烫,产生无色气泡,且产生气泡速率明显加快,铝片上下翻滚。
(1)产生的红褐色沉淀是______________,无色气泡的成分是___________。
(2)生成红褐色沉淀的原因是_____________________________。
(3)写出生成气泡速率明显加快的两个原因____________、_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com