
6g Mg、Cu合金与一定量的硝酸恰好完全反应,收集到标准状况下VL NO和NO2的混合气体。向反应后的溶液中加入足量NaOH溶液,得到沉淀12.12g。则V的值可能是
A.2.688 B.4.48 C.8.064 D.8.96
B
【解析】
试题分析:Mg、Cu都是+2价的金属,失去的电子数与硝酸得到的电子数相等。Mg则变为Mg(OH)2沉淀,Cu变为Cu(OH)2沉淀。因此变为沉淀的OH-的物质的量与电子转移的物质的量相等。沉淀增加的质量即为OH-的质量。n(OH-)=(12.12-6)g÷17g/mol=0.36mol。n(e-)= n(OH-)=0.36mol。若气体完全为NO,则根据电子守恒可的n(NO)=0.36mol÷3×22.4L/mol=2.688L; 若气体完全为NO2,则根据电子守恒可的n(NO2)=0.36mol÷1×22.4L/mol=8.064L.但实际上产生的气体既有NO也有NO2。所以放出气体的体积应该在2.688L~8.064L之间。因此选项为B。
考点:考查极端法在计算金属与硝酸反应中的应用的知识。


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.688 | B、4.48 | C、8.064 | D、8.96 |
查看答案和解析>>
科目:高中化学 来源: 题型:
Mg、Cu合金8.4g完全溶于浓硝酸中,若反应中硝酸被还原,只产生4480mLNO2和2240mLN2O4,反应后的溶液中加足量的NaOH溶液,生成的沉淀再经灼烧后所得固体质量为:
A.15.2 g, B.11.6g C.13.5g, D.16.6 g
【解析】根据反应过程不难判断,生成的沉淀是氢氧化镁和氢氧化铜,灼烧得到的是氧化镁和氧化铜,因为金属每失去2mol电子,就要结合1mol氧原子。硝酸的还原产物是NO2和N2O4,转移的电子是,所以根据得失电子守恒可知,金属结合的氧原子是0.2mol,质量是0.2mol×16g/mol=3.2g,所以最终的固体质量是11.6g。即答案是B。
查看答案和解析>>
科目:高中化学 来源:2013届河北省高二下学期期中考试化学试卷(解析版) 题型:选择题
Mg、Cu合金8.4g完全溶于浓硝酸中,若反应中硝酸被还原,只产生4480mLNO2和2240mLN2O4,反应后的溶液中加足量的NaOH溶液,生成的沉淀再经灼烧后所得固体质量为:
A.15.2 g, B.11.6g C.13.5g, D.16.6 g
【解析】根据反应过程不难判断,生成的沉淀是氢氧化镁和氢氧化铜,灼烧得到的是氧化镁和氧化铜,因为金属每失去2mol电子,就要结合1mol氧原子。硝酸的还原产物是NO2和N2O4,转移的电子是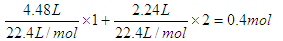 ,所以根据得失电子守恒可知,金属结合的氧原子是0.2mol,质量是0.2mol×16g/mol=3.2g,所以最终的固体质量是11.6g。即答案是B。
,所以根据得失电子守恒可知,金属结合的氧原子是0.2mol,质量是0.2mol×16g/mol=3.2g,所以最终的固体质量是11.6g。即答案是B。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com