
【题目】下列物质中,能够导电的是( )
A. 二氧化碳气体 B. 硫酸溶液 C. 蔗糖溶液 D. 固体氯化钠
科目:高中化学 来源: 题型:
【题目】已知:Kw=1.0×10﹣14 , Al(OH)3AlO2﹣+H++H2O K=2.0×10﹣13 . 则Al(OH)3溶于NaOH溶液反应的平衡常数数值为( )
A.10
B.15
C.20
D.25
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近,科学家用巨型计算机进行模拟化确认,由60个N原子可结合成N60分子,N60变成N2时放出巨大能量,下列说法中不正确的是( )
A. N60与N2都是氮的同素异形体 B. 1个N60分子中含60个N原子
C. N60 的相对分子质量为840,属高分子化合物 D. N60 变成N2的反应是放热反应,说明N2比N60更稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①25 ℃时,弱电解质的电离平衡常数:K(CH3COOH)=1.8×10-5,K(HSCN)=0.13;难溶电解质的溶度积常数:Ksp(CaF2)=6×10-10。②25 ℃时,2.0×10-3 mol/L氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系,如下图所示:
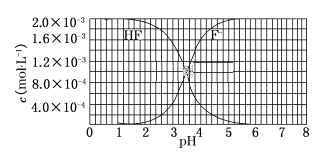
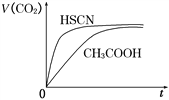
请根据以上信息回答下列问题:
(1)25 ℃时,将20 mL 0.10 mol/L CH3COOH溶液和20 mL 0.10 mol/L HSCN溶液分别与20 mL 0.10 mol/L NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示,反应初始阶段,两种溶液产生CO2气体的速率存在明显差异的原因是__________,反应结束后所得两溶液中,c(CH3COO-)________c(SCN-)(填“>”、“<”或“=”)。
(2)25 ℃时,HF电离平衡常数的数值Ka≈______。
(3)4.0×10-3 mol/L HF溶液与4.0×10-4mol/L CaCl2溶液等体积混合,调节混合液pH为4.0后(忽略调节时混合液体积的变化),_______沉淀产生。(填“有”或“无”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热条件下,硅单质和HCl反应生成SiHCl3是粗硅提纯的重要步骤.某小组设计如图所示装置完成上述转化(夹持装置略去). 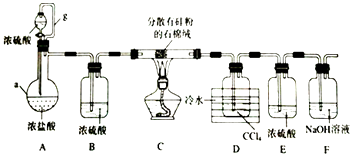
已知:SiHCl3的沸点为33.0°C,易溶于有机溶剂,能与水剧烈反应,在空气中易被氧化,CCl4的沸点为76.8°C.
请回答:
(1)仪器a的名称为;导管g的作用为;
(2)装置A中,浓硫酸体现的性质为;实验时,需先打开分液漏斗活塞,一段时间后,在点燃C处酒精灯,理由是;
(3)装置C中发生反应的化学方程式为;
(4)装置D中所得的液态混合物的分离方法为 . (填操作名称)
(5)反应后的气体通过装置F中的NaOH溶液后,对逸出气体的处理方法为;
(6)SiHCl3在潮湿的空气中被氧化,生成一种氧化物和一种无氧酸,该反应的化学方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液含有较多的Na2SO4和少量的Fe2(SO4)3,若用该溶液制取芒硝,可供选择的操作有
①加适量的H2SO4溶液 ②加金属Na ③结晶 ④加过量NaOH溶液 ⑤加强热脱结晶水 ⑥过滤。正确的操作步骤是
A.②⑥③B.④⑥①③C.④⑥③⑤D.②⑥①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50 mL 0.6 mol·L-1氢氧化钠溶液,含氢氧化钠的物质的量为 ( )
A. 0.03 mol B. 0.04 mol C. 0.05 mol D. 0.06 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com