
���� ��1������������Ũ�����ڼ��������·�Ӧ�����������������������Ԫ�ء��Ȼ�������Ԫ�ػ��ϼ۱仯��Ŀ����ת�Ƶ�������
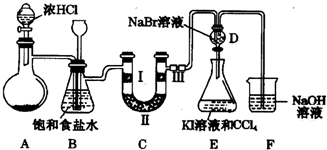
��2��Ũ�����ӷ�����ȡ�������к����Ȼ��⣬�ñ���ʳ��ˮ���������Ȼ��⣻Bװ�û��ܹ����ʵ�������װ��C�Ƿ���������
��3����֤�����Ƿ����Ư���ԣ�Ҫ��֤����������Ư���ԣ�ʪ�����ɫ�����У�������ˮ��Ӧ���ɴ��������Ư���ԣ�
��4�������������廯�Ʒ�Ӧ�����ж����������Դ����嵥�ʣ���Dװ�÷�Һ©���Ļ���������E���嵥�ʺ͵⻯�ط�Ӧ���ɵⵥ�ʣ��ݴ����ʵ�鲽�裻
��5�������ж���ֱ���ŷ�������ɿ�����Ⱦ���������������Ʒ�Ӧ���ܹ��������������գ�
��6������������Һ�� ͨ��������Ӧ���������ƣ�ͬʱ���ɵ�������������Ʒ�Ӧ��������Ⱦ�����������
��� �⣺��1������������Ũ�����ڼ��������·�Ӧ������������ѧ����ʽΪ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
��Aװ���й���ҩƷΪKClO3�������ᷴӦ�Ļ�ѧ����ʽΪ��KClO3+6HCl=KCl+3Cl2��+3H2O����Ӧ����3molCl2��ת�Ƶ���5mol����Ӧ��ÿ����1mol Cl2ʱת�Ƶ��ӵ����ʵ���Ϊ$\frac{5}{3}$��
�ʴ�Ϊ��$\frac{5}{3}$��
��2��Ũ�����ӷ�����ȡ�������к����Ȼ��⣬�Ȼ���������ˮ�������ڱ���ʳ��ˮ���ܽ�Ȳ����ñ���ʳ��ˮ���������Ȼ��⣻
���ʵ�������װ��C�Ƿ�����������C�з����������ῴ�ģ�B�г���©����Һ���������γ�Һ����
�ʴ�Ϊ����ȥ�����е��Ȼ��⣬���ʵ�������װ��C�Ƿ���������
��3��װ��C��ʵ��Ŀ������֤�����Ƿ����Ư���ԣ���֤�����Ƿ����Ư���ԣ�Ҫ��֤����������Ư���ԣ�ʪ�����ɫ�����У�������ˮ��Ӧ���ɴ��������Ư���ԣ�����Ӧ�Ǹ������ˮ�Ȼ��ƣ�ʪ�������ͨ�������ȥˮ�֣�ͨ���������ɫ��������������ɫ��
�ʴ�Ϊ����ˮ�Ȼ��ƣ��������ɫ������
��4���������廯�Ʒ�Ӧ�����ж����������Դ����嵥�ʣ���Dװ�÷�Һ©���Ļ���������E���嵥�ʺ͵⻯�ط�Ӧ���ɵⵥ�ʣ�ʵ�鲽��Ϊ����A�з�Һ©��������һ��ʱ���D�е���ɫ��Һ��Ϊ��ɫ���Ⱥ�ɫ���ɫ����˵���ȵķǽ����Դ����壻��D�л�������D��������Һ����װ��E�У����²�Ϊ�Ϻ�ɫ��˵����ķǽ����Դ��ڵ⣬
�ʴ�Ϊ����A�з�Һ©��������һ��ʱ���D�е���ɫ��Һ��Ϊ��ɫ���Ⱥ�ɫ���ɫ����˵���ȵķǽ����Դ����壻��D�л�������D��������Һ����װ��E�У����²�Ϊ�Ϻ�ɫ��˵����ķǽ����Դ��ڵ⣻
��5�������ж���ֱ���ŷ�������ɿ�����Ⱦ���������������Ʒ�Ӧ�����Ȼ��ơ��������ƺ�ˮ������ʽΪ��Cl2+2NaOH=NaCl+NaClO+H2O��
�ʴ�Ϊ��Cl2+2NaOH=NaCl+NaClO+H2O��
��6������������Һ��ͨ��������Ӧ���������ƣ���Ӧ�����ӷ���ʽΪSO32-+Cl2+H2O=SO42-+2Cl-+2H+��ͬʱ���ɵ�������������Ʒ�Ӧ��������Ⱦ�����������Ӧ�����ӷ���ʽΪSO32-+2H+=SO2��+H2O��
�ʴ�Ϊ��SO32-+Cl2+H2O=SO42-+2Cl-+2H+��SO32-+2H+=SO2��+H2O��
���� ���⿼��������ʵ������ȡ���������ʵļ��顢ʵ����ơ�ʵ��װ�õ��������ۡ���ѧ����ʽ�����ӷ���ʽ����д�ȣ�ע��װ�����ӵIJ�����ʵ����ƣ����ջ����ǹؼ�����Ŀ�Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������Һ��ͨ��������4Fe2++O2+4H+=4Fe3++2H2O | |
| B�� | ��0.3mol/L���Ȼ����Һ��ȥ����������������������þ��Mg��OH��2+2NH4+=Mg2++2NH3•H2O | |
| C�� | ��1mol������ˮ��Һ���м����������������������������ʱ���ӷ���ʽ�Ʊ�ʾΪ��Al3++2SO42-+2Ba2++4OH-=2BaSO4��+AlO2-+2H2O | |
| D�� | ���Ը�����غ���������ȡ����������4MnO4-+4H2O2+12H+=4Mn 2++7O2��+10H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ۢ� | B�� | �ڢܢ� | C�� | �٢ڢ� | D�� | �ڢۢ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com