
| A、87.5% |
| B、12.5% |
| C、14.3% |
| D、85.7% |
| 56m |
| 64 |
| 7m |
| 8 |
| 7m |
| 8 |
| ||
| mg |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
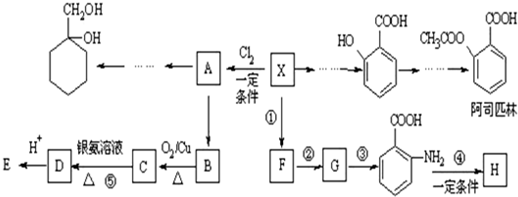
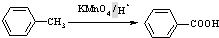
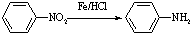 (苯胺,易被氧化)
(苯胺,易被氧化)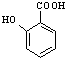 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有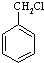 和其他无机物合成
和其他无机物合成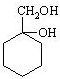 最合理的方案(不超过4步),请在答题纸的方框中表示.例:
最合理的方案(不超过4步),请在答题纸的方框中表示.例: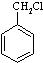
| 反应物 |
| 反应条件 |
| 反应物 |
| 反应条件 |
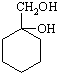
查看答案和解析>>
科目:高中化学 来源: 题型:
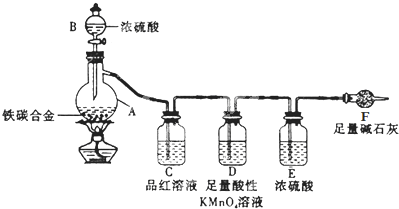
查看答案和解析>>
科目:高中化学 来源: 题型:
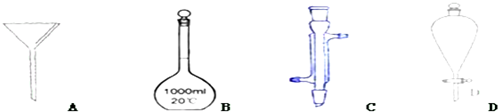
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、R表示处方药,OTC表示非处方药 |
| B、毒品就是有毒的药品 |
| C、我国明代医学家李时珍所著的医学名著是《神农本草经》 |
| D、麻黄碱是国际奥委会严格禁止使用的兴奋剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
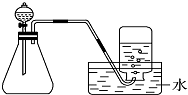 下列制取气体的方案,可以直接采用如图所示装置进行的是
下列制取气体的方案,可以直接采用如图所示装置进行的是| A、①④ | B、②③④ |
| C、①②⑤ | D、①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com