
| A. | 胆矾、漂白粉、氯化钾、硫酸钡 | B. | 盐酸、空气、硝酸、干冰 | ||
| C. | 冰醋酸、海水、氧化铝、乙醇 | D. | 蛋白质、油脂、烧碱、石灰石 |
分析 根据纯净物是一种物质组成的物质;
混合物是不同物质组成的物质;
电解质是水溶液中或熔融状态下都导电的化合物;
非电解质是水溶液中和熔融状态下都不导电的化合物.
解答 解:A.胆矾、漂白粉、氯化钾、硫酸钡分别属于化合物、混合物、电解质、电解质故A错误;
B.盐酸、空气、硝酸、干冰分别属于混合物、混合物、电解质、非电解质,故B错误;
C.冰醋酸、海水、氧化铝、乙醇分别属于纯净物、混合物、电解质、非电解质,故C正确;
D.蛋白质、油脂、烧碱、石灰石分别属于混合物、混合物、电解质、电解质,故D错误.
故选C.
点评 本题考查纯净物、混合物、电解质和非电解质的概念,需要对相关概念有深刻的理解,并能对相关属类的物质有清晰的理解,这要求在学习概念时,既要理解概念,又要能举出典型例子.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 利用装置①可制备氢氧化亚铁并长时间观察其颜色 | |
| B. | 装置②中X若为四氯化碳,可用于吸收HCl气体,并防止倒吸 | |
| C. | 装置③验证Na2CO3和NaHCO3两种固体的热稳定性 | |
| D. | 通过④的方法配制一定浓度的稀硫酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 澄清透明的溶液中:MnO${\;}_{4}^{-}$、SO${\;}_{4}^{2-}$、K+、Fe3+ | |
| B. | 加入铝粉产生氢气的溶液:Na+、K+、SO42-、Cl- | |
| C. | 使pH试纸变红的溶液中:NH4+、Cu2+、SO42-、Cl- | |
| D. | 0.1mol•L-1CH3COONa溶液中:H+、Ca2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
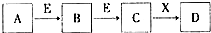 中学常见物质A、B、C、D、E、X,存在下图转化关系(部分生成物和反应条件略去).下列推断不正确的是( )
中学常见物质A、B、C、D、E、X,存在下图转化关系(部分生成物和反应条件略去).下列推断不正确的是( )| A. | 若D为NaCl,且A可与C反应生成B,则E可能是CO2 | |
| B. | 若D是一种强碱,则A、B、C均可与X反应生成D | |
| C. | 若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C | |
| D. | 若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C(s)+$\frac{1}{2}$O2(g)=CO(g);△H=-393.5 kJ/mol | |
| B. | 2H2(g)+O2(g)=2H2O(g);△H=+571.6 kJ/mol | |
| C. | CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890.3 kJ | |
| D. | $\frac{1}{2}$C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l);△H=-1400 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 存在的电离有:HCO${\;}_{3}^{-}$+H2O═H2CO3+OH- | |
| B. | c(Na+)+c(H+)=c(HCO${\;}_{3}^{-}$)+2c(CO${\;}_{3}^{2-}$)+c (OH-) | |
| C. | HCO${\;}_{3}^{-}$的电离程度大于HCO${\;}_{3}^{-}$的水解程度 | |
| D. | c(Na+)═c(HCO${\;}_{3}^{-}$)+c (CO${\;}_{3}^{2-}$)+2c(H2CO3) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com