
分析 某气态烃10mL,通入氧气100mL,宪全燃烧后.冷却致室温,体积变为75mL,再通过足量的石灰水后,干燥,气体的体积变为35mL,说明生成40mLCO2,则有机物含有4个C原子,结合有机物燃烧的化学方程式利用差量法计算.
解答 解:某气态烃10mL,通入氧气100mL,宪全燃烧后.冷却致室温,体积变为75mL,再通过足量的石灰水后,干燥,气体的体积变为35mL,说明生成40mLCO2,则有机物含有4个C原子,
设分子式为C4Hx,则C4Hx+(4+$\frac{x}{4}$)O2→4CO2+$\frac{x}{2}$H2O△V
1 4+$\frac{x}{4}$ 4 1+$\frac{x}{4}$
10ml (10+100)mL-75mL
解之得x=10,
则分子式为C4H10,
故答案为:C4H10.
点评 本题考查了有机物分子式的计算,侧重考查学生的分析、计算能力,题目难度中等,明确气体减少的原因及组成为解答关键,注意掌握差量法、质量守恒定律在化学计算中的应用方法.


科目:高中化学 来源: 题型:选择题
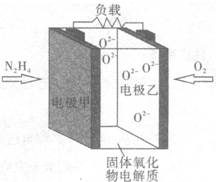 液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.某科研人员设计了以液态肼(N2H4)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池(如图所示).该固体氧化物电解质的工作温度高达700~900℃时,O2-可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质.下列说法正确的是( )
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.某科研人员设计了以液态肼(N2H4)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池(如图所示).该固体氧化物电解质的工作温度高达700~900℃时,O2-可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质.下列说法正确的是( )| A. | 电极甲为电池正极 | |
| B. | 电池总反应为N2H4+2O2═2NO+2H2O | |
| C. | 电池正极反应式为O2+2H2O+4e-═4OH- | |
| D. | 图示中的O2-由电极乙移向电极甲 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 操作和现象 | 结论 |
| A | 向某溶液中先滴加稀硝酸,再滴加Ba(NO3)2溶液,出现白色沉淀 | 该溶液中一定含有SO42- |
| B | 向某溶液中加入足量浓NaOH溶液并微热,产生能使湿润的红色石蕊试纸变蓝的无色气体 | 该溶液中含NH4+ |
| C | 常温下,测得饱和NaA溶液的pH大于饱和NaB溶液 | 常温下水解程度:A->B- |
| D | 向蔗糖溶液中滴加少量稀H2SO4,水浴加热;向其中滴加少量新制Cu(OH)2悬浊液,加热,无明显现象 | 蔗糖没有水解 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 今有正反应放热的可逆反应,若反应开始经t1后达平衡,在t2时由于反应条件改变,使平衡破坏,到t3时又达平衡,如图所示.
今有正反应放热的可逆反应,若反应开始经t1后达平衡,在t2时由于反应条件改变,使平衡破坏,到t3时又达平衡,如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸被稀释时只有水合过程,所以浓硫酸稀释时放热 | |
| B. | 氯化铵晶体投入水中只有扩散过程,所以氯化铵晶体溶于水吸热 | |
| C. | 烧碱溶于水,溶液温度升高,说明烧碱溶解时水合过程放出的热量大于扩散过程吸收的热量 | |
| D. | 任何物质溶于水,要么温度升高,要么温度下降 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑥ | B. | ①③④ | C. | ①③ | D. | ⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com