
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1:1 |
| c | 化学组成为BDF2 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
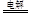 2OH- +H2↑+C12↑(或2NaCl(熔融)
2OH- +H2↑+C12↑(或2NaCl(熔融)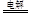 2Na+Cl2。↑(每空2分)
2Na+Cl2。↑(每空2分)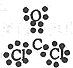 (1分) 金属晶体(1分)
(1分) 金属晶体(1分)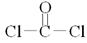 ,据此便可写出其电子式
,据此便可写出其电子式 ;只存在一种类型作用力且可导电的单质晶体为金属钠,属于金属晶体。
;只存在一种类型作用力且可导电的单质晶体为金属钠,属于金属晶体。

科目:高中化学 来源:不详 题型:单选题
 是重要的核工业原料,但在自然界的丰度很低,
是重要的核工业原料,但在自然界的丰度很低, 的浓缩一直为国际社会关注。下列有关:
的浓缩一直为国际社会关注。下列有关: 说法正确的是
说法正确的是 与
与 互为同位素
互为同位素 原子核外有143个电子
原子核外有143个电子 与
与 是同一种核素
是同一种核素 原子核中含有92个中子
原子核中含有92个中子查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.钡可从氯化钠溶液中置换出金属钠 |
| B.钡可从冷水中置换出氢气 |
| C.钡可从硫酸铜溶液中置换出铜 |
| D.在溶液中Ba2+可氧化金属锌,生成Zn2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.热稳定性:HCl> HI | B.原子半径:Na> Mg |
| C.酸性:H2SO3>H2SO4。 | D.结合质子能力:S2-> Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
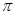 键的数目为 。
键的数目为 。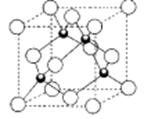
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
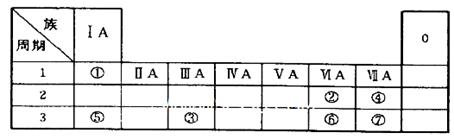
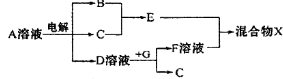
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com