
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.①③④ | B.②⑤⑥ | C.④⑥ | D.①⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.锂在过量氧气中燃烧的产物是氧化锂而不是过氧化锂 |
| B.碳酸锂的溶解度比碳酸氢锂大 |
| C.碳酸锂受强热能分解成Li2O和CO2 |
| D.锂和水的反应不如钠和水的反应剧烈 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属锂保存在煤油中,使用前要用滤纸吸干煤油 |
| B.过氧化钠比氧化钠稳定,可露置在空气中 |
| C.称量NaOH固体时,可在天平两个托盘上各放一张等质量的纸,左边纸上放NaOH,右边纸上放砝码 |
| D.做焰色反应实验时,透过蓝色钴玻璃,观察到火焰颜色为紫色,证明被检验物中一定有钾元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.①③ | C.①④ | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

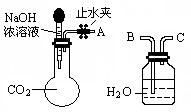
| 实验操作 | 实验现象 | 结论 | |
| ① 取少量白色固体于试管中,加足量水溶解,再加足量BaCl2溶液 | | | |
| ② 过滤,取2 mL滤液于试管中 | |||
| ③ | | | |
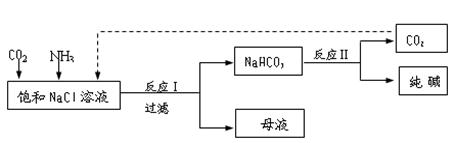
 NaHCO3↓+NH4Cl,处理母液的两种方法如下。
NaHCO3↓+NH4Cl,处理母液的两种方法如下。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.热稳定性:Na2CO3<NaHCO3 |
| B.相同温度下在水中的溶解度:Na2CO3<NaHCO3 |
| C.等质量的两种固体,分别与过量盐酸反应,生成CO2的质量相等 |
| D.取1mol?L-1的两种溶液,分别滴入酚酞,溶液颜色较深的是Na2CO3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com