
 ά����C�ֽп���Ѫ�ᣬ��һ��ˮ����ά���أ��ڿ����м��������ױ��������ⵥ���ܽ�����������ṹ����ʾ��
ά����C�ֽп���Ѫ�ᣬ��һ��ˮ����ά���أ��ڿ����м��������ױ��������ⵥ���ܽ�����������ṹ����ʾ������ ��1�����ݽṹ��ʽ��д����ʽ��
��2��ά����C�ڿ����м��������ױ�����������ʧȥӪ����ֵ��
��3���ⵥ���ܽ�ά����C���������Լ���ⵥ���Ƿ���������֤������ˮ������ά����C��
��4��a�����岻�ܺϳ�ά���أ�
b��ά����C������Ȼ�����ʣ�ҩ���Ǻϳɵ����ʣ����߽�Ȼ��ͬ��
c�������и���ά����C��
��� �⣺��1������ά����C�Ľṹ��ʽ��д����ʽΪ��C6H8O6���ʴ�Ϊ��C6H8O6��
��2��ά����C�ڿ����м��������ױ����������������߲˱�����߲˺ã��ʴ�Ϊ��ά����C����ʱ�����ױ�������
��3���ⵥ���ܽ�ά����C���������õⵥ�������۱���ɫ�����������飬���Խ�����ˮ�����ó�֭��ȡ������ˮ���Թ��У��Ӽ��ε�����Һ������ɫ��Ȼ���ˮ��֭����ɫ��dz����ȥ��֤������ˮ������ά����C���ʴ�Ϊ��������ˮ�����ó�֭��ȡ������ˮ���Թ��У��Ӽ��ε�����Һ������ɫ��Ȼ���ˮ��֭����ɫ��dz����ȥ��
��4��a�����岻�ܺϳ�ά���أ�ֻ�ܴ�ˮ���߲��л�ȡ����a����
b��ά����C������Ȼ�����ʣ�ҩ���Ǻϳɵ����ʣ����߽�Ȼ��ͬ��ά����C���ܱ������ݣ���b����
c�������и���ά����C���ױ������е�������������c��ȷ��
��ѡc��
���� ���⿼��ά�����������е����ã���һ����ѧ���������ϵ���Ŀ�����Ը�����ѧ֪ʶ���лش��ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
��| Ԫ�ط��� | �����Ų�ʽ | �۲�����Ų� | �����ڱ��е�λ�� |
| �� | 1s22s22p6 | �� | �� |
| Cr | �� | �� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��Դ���ִ���ᷢչ��֧��֮һ����ѧ������Ҫ����Դ��
��Դ���ִ���ᷢչ��֧��֮һ����ѧ������Ҫ����Դ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
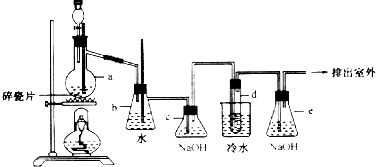
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeCl2 | B�� | H2SiO3 | C�� | NH4NO3 | D�� | HCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �۱�ϩ�Ľṹ��ʽ��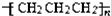 | B�� | �Ҵ��Ľṹ��ʽ��CH3CH2OH | ||
| C�� | ���Ȼ�̼�ĵ���ʽ��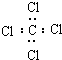 | D�� | -CH3�������ĵ���ʽΪ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶 Z��Y��X | |
| B�� | Z�ķǽ�������ǿ | |
| C�� | �⻯�ﻹԭ��XH3��H2Y��HZ���ȶ���XH3��H2Y��HZ | |
| D�� | ����������Ӧˮ����H3XO4������ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
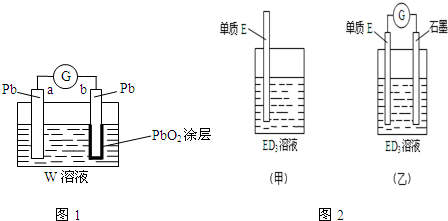
��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com