
【题目】甲同学通过查询资料知道,一定浓度的硝酸与镁反应时,可得到二氧化氮、一氧化氮、氮气三种气体。该同学用下列仪器组装装置来直接验证有二氧化氮、一氧化氮生成并制取氮化镁 (假设实验中每步转化均是完全的) 。查阅文献得知:
①二氧化氮沸点为21.1 ℃、熔点为-11 ℃,一氧化氮沸点为-151 ℃、熔点为-164 ℃;
②镁也能与二氧化碳反应;
③氮化镁遇水反应生成氢氧化镁和氨气。
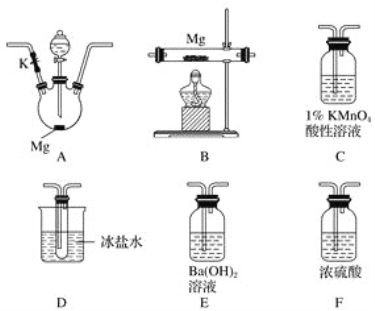
(1)实验中先打开开关K,通过导管向装置内通入二氧化碳气体以排出装置内的空气,停止通入二氧化碳的标志是________________________________。
(2)为实现上述实验目的,所选用的仪器的正确连接方式是A→____________→E,确定还原产物中有二氧化氮的现象是______________________________________,实验中要多次使用装置F,第二次使用F的目的是______________________________________________。
(3)实验过程中,发现在D中产生预期现象的同时,C中溶液颜色慢慢褪去,试写出C中反应的离子方程式:________________________________。
(4)甲同学在A中开始反应时,马上点燃B处的酒精灯,实验结束后通过测试发现B处的产品纯度不高,原因是______________________________________。
(5)设计一种实验方案,验证镁与硝酸反应时确实有氮气生成:__________________________。
【答案】(1)E中出现白色沉淀(2)D→C→F→B→F
A中有红棕色气体产生(或D中出现有色液体) 防止水蒸气进入B导致氮化镁水解
(3)5NO+4H++3Mn![]() ===3Mn2++5N
===3Mn2++5N![]() +2H2O
+2H2O
(4)装置中充满CO2,而加热时CO2也能与Mg反应
(5)取少量B中反应后的固体放入试管中,再向试管中滴加适量的水并将湿润的红色石蕊试纸靠近试管口处,试纸变蓝
【解析】
探究一定浓度的硝酸与Mg反应产物:A三颈烧瓶中为镁和硝酸反应,可能得到NO2、NO、N2三种气体,若产生二氧化氮气体,A中有红棕色气体产生,NO2沸点为21.1℃,经过D装置冰盐水冷却生成的气体,D中出现有色液体,C中盛放1%的酸性高锰酸钾,若出现高锰酸钾褪色,说明有NO生成,经过装置F进行气体干燥,然后进入装置B进行镁和氮气的反应,再经过装置F,防止水蒸气进入B导致氮化镁水解,最后用氢氧化钡吸收尾气,据此解答。
(1)探究一定浓度的硝酸与Mg反应产物,E装置在该实验中为吸收尾气装置,实验中先打开开关K,通过导管向装置内通入CO2气体以排出装置内的空气,当E中出现白色沉淀,说明二氧化碳已经充满整个装置,已经全部排出装置内的空气,需停止通入CO2;
(2)探究一定浓度的硝酸与Mg反应产物:A三颈烧瓶中为镁和硝酸反应,可能得到NO2、NO、N2三种气体,若有二氧化氮气体产生,A中有红棕色气体产生,经过D装置冰盐水冷却生成的气体,D中出现有色液体,C中盛放1%的酸性高锰酸钾,若出现高锰酸钾褪色,说明有NO生成,反应为:5NO+4H++3MnO4-=3Mn2++5NO3-+2H2O,经过装置F进行气体干燥,然后进入装置B进行镁和氮气的反应,再经过装置F,防止空气中的水蒸气进入B导致氮化镁水解,最后用氢氧化钡吸收尾气,所选用的仪器的正确连接方式是:A→D→C→F→B→F→E,氮化镁易水解,第二次使用F的目的是防止空气中的水蒸气进入B导致氮化镁水解;
(3)C中溶液颜色慢慢褪去,为NO和高锰酸根离子发生的氧化还原反应,该反应中物质的化合价变化:MnO4-→Mn2+,Mn元素化合价由+7价→+2价,一个MnO4-得5个电子;NO→NO3-,N由+2价变成+5价,一个NO分子失去3个电子,所以其最小公倍数为15,故MnO4-的计量数为3,NO的计量数为5,然后根据原子守恒配平其它元素,配平后的离子方程式为5NO+4H++3MnO4-=3Mn2++5NO3-+2H2O;
(4)镁条与二氧化碳发生置换反应,生成碳与氧化镁,反应为2Mg+CO2![]() 2MgO+C,所以在A中开始反应时,马上点燃B处的酒精灯,实验结束后通过测试发现B处的产品纯度不高,原因是装置中充满CO2,而加热时CO2也能与Mg反应;
2MgO+C,所以在A中开始反应时,马上点燃B处的酒精灯,实验结束后通过测试发现B处的产品纯度不高,原因是装置中充满CO2,而加热时CO2也能与Mg反应;
(5)镁与硝酸反应时若有氮气生成,则生成的氮气和镁反应生成氮化镁,氮化镁易水解生成氨气,所以取少量B中反应后的固体放入试管中,再向试管中滴加适量的水并将湿润的红色石蕊试纸靠近试管口处,试纸变蓝,则检验到氨气,说明镁和硝酸反应有氮气生成。


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案科目:高中化学 来源: 题型:
【题目】有三种物质AC2、B2C2、AD4,元素A在自然界中形成的物质种类最多;元素B的单质能在C的气态单质中剧烈燃烧,火焰呈黄色,并生成淡黄色固体B2C2;元素D的负一价阴离子的电子层结构与氩原子相同,则:
(1)A、B、C、D的元素名称分别是________、________、________、________。
(2)AD4分子中含有的共价键类型为________(填“σ键”或“π键”)。
(3)D的负一价阴离子的电子排布式为________,B2C2的电子式为________,属________(填“离子化合物”或“共价化合物”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
X | L层p电子数比s电子数多2个 |
Y | 第三周期元素的简单离子中半径最小 |
Z | L层有三个未成对电子 |
(1)写出元素X的离子结构示意图__________。
(2)写出Y元素最高价氧化物的水化物分别与HCl、NaOH溶液反应的离子方程式_______________________、_________________________。
(3)写出Z与Y的电子排布式______________、________________。
(4)元素T与氯元素相比,非金属性较强的是__________(用元素符号表示),下列表述中能证明这一事实的是__________。
A.气态氢化物的挥发性和稳定性
B.单质分子中的键能
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中X—H键的键长(X代表T和Cl两种元素)
F.两单质在自然界中的存在形式
(5)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是__________(填元素符号),理由是________________________________________________。
【答案】 ![]() Al(OH)3+3H+===Al3++3H2O Al(OH)3+OH-===AlO
Al(OH)3+3H+===Al3++3H2O Al(OH)3+OH-===AlO![]() +2H2O 1s22s22p3 1s22s22p63s23p1 F CE Al 具有金属性
+2H2O 1s22s22p3 1s22s22p63s23p1 F CE Al 具有金属性
【解析】试题分析:T单质能与水剧烈反应,所得溶液呈弱酸性,所以T是F元素;X元素的L层p电子数比s电子数多2个,X元素是O元素;Y元素是第三周期元素的简单离子中半径最小,Y是Al元素;Z元素L层有三个未成对电子,Z是N元素;
解析:根据以上分析,(1)X为O元素,氧离子核外最外层达到8电子稳定结构,氧离子结构示意图![]() 。
。
(2)Y元素最高价氧化物水化物Al(OH)3,为两性氢氧化物,与盐酸反应生成氯化铝和水,离子方程式为Al(OH)3+3H+===Al3++3H2O;与氢氧化钠溶液反应生成偏铝酸钠和水,离子方程式为Al(OH)3+OH-===AlO![]() +2H2O;
+2H2O;
(3)Z是N元素,电子排布式是1s22s22p3; Y是Al元素,电子排布式是1s22s22p63s23p1。
(4)T是F元素,同主族元素从上到下,非金属性减弱,与氯元素相比,非金属性较强的是F;
A.气态氢化物的挥发性不能证明非金属性的强弱,故A错误;
B.单质分子中的键能,不能证明非金属性的强弱,故B错误;
C.非金属性越强,电负性越大,根据两元素的电负性可以判断非金属性,故C正确;
D.根据最高价含氧酸的酸性可以判断非金属性,故D错误;
E.键长越长,越不稳定,
F.单质在自然界中的存在形式,不能判断非金属性,故F错误。
(5)Al为金属元素,具有金属性,其它三种元素为非金属元素,具有较强的非金属性。
点睛:元素非金属性强弱的判断方法:①越易与氢气化合,非金属性越强;②气态氢化物越稳定,非金属性越强;③单质的氧化性越强,非金属性越强;④最高价含氧酸的酸性越强,非金属性越强。
【题型】综合题
【结束】
21
【题目】下表是元素周期表前五周期的一部分,X、Y、Z、R、W、J是6种元素的代号。其中J为0族元素。
X | Y | Z | |
R | |||
W | |||
J |
请回答下列问题(除特别说明外,凡涉及用元素回答的问题均用具体元素符号表示):
(1)R原子的电子排布图为__________。
(2)在化合物YZ2中Y的化合价为__________;Y2-与Na+的半径大小为__________。
(3)在X、Y、Z三种元素中,电负性由大到小的顺序是__________;X与Y的第一电离能:X__________Y(填“<”、“>”或“=”),其理由是__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
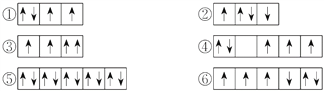
【题目】(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况,试判断哪些违反了泡利原理__________,哪些违反了洪特规则__________。
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为__________;其最高价氧化物对应水化物的化学式是__________。
(3)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列。
①2s ②3d ③4s ④3s ⑤4p ⑥3p
轨道能量由低到高排列顺序是__________。
【答案】 ③ ②④⑥ 1s22s22p63s23p4 H2SO4 ①④⑥③②⑤
【解析】试题分析:(1)在一个原子轨道里,最多只能容纳2个电子,而且它们的自旋状态相反,称为泡利不相容原理;当电子排布在同一个能级的不同轨道时,基态原子中的电子总是单独优先占据一个轨道,而且自旋状态相同,称为洪特规则;(2)根据激发态原子核外电子排布式知该元素核外有16个电子,根据能量最低原理分析其基态原子核外电子排;(3)相同电子层上原子轨道能量的高低:ns<np<nd;形状相同的原子轨道能量的高低:1s<2s<3s<4s……。
解析:(1)在一个原子轨道里,最多只能容纳2个电子,而且它们的自旋状态相反,称为泡利不相容原理,所以违反泡利不相容原理的有③;当电子排布在同一个能级的不同轨道时,基态原子中的电子总是单独优先占据一个轨道,而且自旋状态相同,称为洪特规则,所以违反洪特规则的有②④⑥;(2)根据激发态原子核外电子排布式知该元素核外有16个电子,为S元素;根据能量最低原理,其基态原子核外电子排是1s22s22p63s23p4;S元素最外层有6个电子,所以最高价是+6价,最高价氧化物对应水化物的化学式是H2SO4;(3)相同电子层上原子轨道能量的高低:ns<np<nd;形状相同的原子轨道能量的高低:1s<2s<3s<4s……,多电子原子的原子轨道按轨道能量由低到高顺序是①④⑥③②⑤。
【题型】综合题
【结束】
18
【题目】四种短周期元素A、B、C、D的性质或结构信息如下。
信息①:原子半径大小:A>B>C>D
信息②:四种元素之间形成的某三种分子的比例模型及部分性质:
|
|
|
是地球上最常见的物质之一,常温为液态,是包括人类在内所有生命生存的重要资源,也是生物体最重要的组成部分 | 无色,无味且易燃,是21世纪的主要能源 | 弱酸,有强氧化性,可以用于消毒杀菌 |
请根据上述信息回答下列问题。
(1)甲、乙、丙中含有的共同元素是 (填名称)。
(2)B元素在周期表中的位置为 。
(3)上述元素的原子M层有一个未成对p电子的是 (填元素符号)。
(4)丙的电子式为 ,丙与SO2水溶液可发生氧化还原反应,生成两种强酸,化学反应方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列行为中符合安全要求的是
A.进入煤矿井时,用火把照明B.用点燃的火柴在液化气钢瓶口检验是否漏气
C.节日期间,在开阔地燃放烟花爆竹D.在实验时,将水倒入浓硫酸中进行稀释
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室里使稀盐酸与锌起反应,在标准状况时生成5.6 L氢气,计算
(1)需要锌的物质的量____?
(2)需要2 mol/L的盐酸多少mL____ ?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com