
(16分)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:
2KMnO4+16HCl(浓) 2KCl + 2MnCl2 + 5Cl2↑ +8H2O
(1)用单线桥法标出电子转移的方向和数目。
(2)该反应中的氧化剂与还原剂物质的量之比是 。
(3)KMnO4的氧化性比Cl2的氧化性 (选填“强”或“弱”)。
(4)如反应中转移了2mol电子,则产生的Cl2在标准状况下体积为 L。
(5)某同学欲用KMnO4固体配制100 mL0.5mol.L-1的溶液。回答下列问题:
①配制KMnO4溶液时需用的主要仪器有托盘天平、药匙、烧杯、玻璃棒、量筒、 、 。
②应用托盘天平称取KMnO4固体 g。
③不规范的实验操作会导致实验结果的误差。分析下列操作对实验结果的影响偏小的是(请填序号) 。
A.加水定容时俯视刻度线
B.容量瓶内壁附有水珠而未干燥处理
C.颠倒摇匀后发现凹液面低于刻度线又加水补上
D.在溶解过程中有少量液体溅出烧杯外
(1)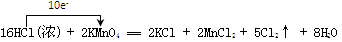 (2)1:5 (3)强
(2)1:5 (3)强
(4)22.4 (5)①胶头滴管 100mL容量瓶 ②7.9g ③CD
【解析】
试题分析:(1)单线桥法表示电子转移是由还原剂指向氧化剂,则高锰酸钾是氧化剂,浓盐酸是还原剂
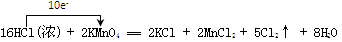
(2)化合价升高元素所在的反应物是还原剂,化合价降低元素所在的反应物是氧化剂;反应2KMnO4 +16HCl(浓)═2KCl+2MnCl2 +5Cl2↑+8H2O中,化合价升高的Cl元素所在的HCl反应物是还原剂,16HCl作还原剂的是10HCl,化合价降低的Mn元素所在的反应物KMnO4 是氧化剂,该反应中的氧化剂与还原剂物质的量之比是1:5;
(3)根据氧化剂的氧化性大于氧化产物的氧化性,则KMnO4的氧化性比Cl2的氧化性强;
(4)反应2KMnO4 +16HCl(浓)═2KCl+2MnCl2 +5Cl2↑+8H2O中,生成5molL氯气,只有10mol盐酸被氧化,转移电子为10mol,当有2mol电子发生转移时,则有1molCl2生成,体积为标况下22.4L。
(5)①配制溶液需要的仪器有托盘天平、药匙、烧杯、玻璃棒、100ml的容量瓶、胶头滴管,则配制KMnO4溶液时需用的主要仪器有托盘天平、药匙、烧杯、玻璃棒、量筒、胶头滴管 、100mL容量瓶。
②需KMnO4固体的质量为m=0.1L×0.5mol?L-1×158g/mol=7.9g 。
③A.加水定容时俯视刻度线,导致水加少了,所配溶液浓度偏高,错误;B.容量瓶内壁附有水珠而未干燥处理,无影响,错误;C.颠倒摇匀后发现凹液面低于刻度线又加水补上,导致水加多了,所配溶液浓度偏低,正确;D.在溶解过程中有少量液体溅出烧杯外,导致溶质减少,所配溶液浓度偏低,错误;选CD。
考点:考查氧化还原反应,溶液的配制等知识。


科目:高中化学 来源:2014-2015广东省高二上学期期中联考化学(文)试卷(解析版) 题型:?????
关于铁丝在氧气中燃烧、铁丝生锈的说法正确的是
A.铁丝燃烧产生白烟 B.铁丝生锈是缓慢氧化
C.铁丝燃烧的产物是Fe2O3 D.铁锈的主要成分是Fe3O4
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省高二上学期期中联考化学(文)试卷(解析版) 题型:?????
对于元素周期表和元素周期律的发现有突出贡献的科学家是
A.拉瓦锡 B.阿伏加德罗
C.门捷列夫 D.道尔顿
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省高二上学期期中联考化学(理)试卷(解析版) 题型:选择题
巴豆酸的结构简式为CH3—CH=CH—COOH。现有①氯化氢、②溴水、③纯碱溶液、④2?丁醇、⑤酸性KMnO4溶液,试根据巴豆酸的结构特点,判断在一定条件下,能与巴豆酸反应的物质是
A.只有②④⑤ B.只有①③④ C.只有①②③④ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省高二上学期期中联考化学(理)试卷(解析版) 题型:选择题
下列表示方法正确的是
① H2S分子的比例模型: ② NH4Cl电子式:
② NH4Cl电子式:
③ 苯乙醛结构简式:  ④ 丙烷分子的球棍模型:
④ 丙烷分子的球棍模型:
A.①④ B.①②④ C.①②③④ D.②③
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省汕头市高一上学期10月月考化学试卷(解析版) 题型:选择题
下列离子方程式改写成化学方程式正确的是
A.Cu2+ + 2OH- = Cu(OH)2↓ CuSO4+Ba(OH)2= Cu(OH)2↓+ Ba2SO4↓
B.CO32- + 2H+ = CO2↑+ H2O NaHCO3 + HCl =NaCl+ CO2↑+ H2O
C.H+ +OH- = H2O NaOH+HNO3=NaNO3+H2O
D.SO42-+Ba2+=BaSO4↓ BaCl2+H2SO4=BaSO4↓+2HCl
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省汕头市高一上学期10月月考化学试卷(解析版) 题型:选择题
用1L1mol·L-1NaOH溶液吸收0.6molCO2,所得溶液中Na2CO3和NaHCO3的物质的量之比约为
A、2︰3 B、1︰2 C、2︰1 D、3︰2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省江南十校高三上学期期末联考理综化学试卷(解析版) 题型:选择题
将H2S通入FeCl3 溶液中,过滤后将反应液加入电解槽中电解(如下图所示)电解后的溶液还可以循环利用。该方法可用于处理石油炼制过程中产生的H2S废气。

下列有关说法正确的是
A.过滤得到的沉淀可能是FeS和S
B.若有0.20mol的电子转移,一定能得到2.24L的氢气
C.可以用Fe与外接电源的a极相连
D.与a极相连的电极反应为Fe2+-2e-=Fe3+
查看答案和解析>>
科目:高中化学 来源:2015年湖北省荆门市高三元月调考理综化学试卷(解析版) 题型:选择题
下表是3种物质的溶解度(20 ℃),下列说法中正确的是
物质 | MgCl2 | Mg(OH)2 | MgCO3 |
溶解度(g/100 g) | 74 | 0.000 84 | 0.01 |
A.已知MgCO3的Ksp=6.82×10-6 mol2·L-2,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)·c(CO32-)=6.82×10-6 mol2·L-2
B.除去粗盐中含有的MgCl2杂质,最佳除杂试剂为Na2CO3溶液
C.将表中三种物质与水混合,加热、灼烧,最终的固体产物相同
D.用石灰水处理含有Mg2+和HCO3-的硬水,发生的离子反应方程式为Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+MgCO3↓+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com