
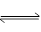
 H2(g)+I2(g)在密闭容器中进行,当__________不随时间变化时,才能说明反应已达到平衡( )
H2(g)+I2(g)在密闭容器中进行,当__________不随时间变化时,才能说明反应已达到平衡( )| A.容器内压强 | B.平均相对分子质量 |
| C.各成分含量 | D.混合气体颜色 |
 H2(g)+I2(g)在密闭容器中进行,因为该反应是气体数不变的反应,故从反应开始到结束,容器的压强都不变,故A不能选;因为该反应是气体数不变的反应,故从反应开始到结束,容器内的平均相对分子质量不变,故B不能选;当各组分的含量和混合气体的颜色不随时间变化时,这说明了反应已经达到平衡,故本题的答案选择CD。
H2(g)+I2(g)在密闭容器中进行,因为该反应是气体数不变的反应,故从反应开始到结束,容器的压强都不变,故A不能选;因为该反应是气体数不变的反应,故从反应开始到结束,容器内的平均相对分子质量不变,故B不能选;当各组分的含量和混合气体的颜色不随时间变化时,这说明了反应已经达到平衡,故本题的答案选择CD。

 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源:不详 题型:单选题
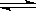 2NO(g)+ O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是 ( )
2NO(g)+ O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是 ( ) | A.①⑤ | B.①②③⑤ | C.①③④ | D.①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 R(g)+S(g),下列说法中可以充分说明这一反应已经达到平衡状态的是
R(g)+S(g),下列说法中可以充分说明这一反应已经达到平衡状态的是| A.P、Q、R、S的浓度相等 | B.P、Q、R、S在容器中共存 |
| C.P、Q、R、S的浓度不再变化 | D.P、Q的消耗速率相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.K值越大,正反应进行的程度越大 |
| B.一般地说,K>105时,该反应进行得就基本完全了 |
| C.压强越大,K值越大 |
| D.K与反应物或生成物的浓度变化无关 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3(g)。达平衡时容器中SO3的物质的量浓度为0.4mol/L,还剩余氧气3.0mol。
2SO3(g)。达平衡时容器中SO3的物质的量浓度为0.4mol/L,还剩余氧气3.0mol。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 TaI4(g)+S2(g) △H﹥0 (Ⅰ)反应(Ⅰ)的平衡常数表达式K= ,若K=1,向某恒容密闭容器中加入1mol I2(g)和足量TaS2(s),I2(g)的平衡转化率为 ,
TaI4(g)+S2(g) △H﹥0 (Ⅰ)反应(Ⅰ)的平衡常数表达式K= ,若K=1,向某恒容密闭容器中加入1mol I2(g)和足量TaS2(s),I2(g)的平衡转化率为 ,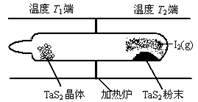
 HSO3-+H+的电离常数Ka=1×10-2mol/L,则该温度下NaHSO3的水解平衡常数Kh= mol/L,若向NaHSO3溶液中加入少量的I2,则溶液中
HSO3-+H+的电离常数Ka=1×10-2mol/L,则该温度下NaHSO3的水解平衡常数Kh= mol/L,若向NaHSO3溶液中加入少量的I2,则溶液中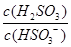 将 (填“增大”“减小”或“不变”)。
将 (填“增大”“减小”或“不变”)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C(g)+D,A和C均为无色气体,当反应达到平衡时,下列叙述不正确的是( )
C(g)+D,A和C均为无色气体,当反应达到平衡时,下列叙述不正确的是( )| A.增大A的浓度,平衡体系颜色加深,则说明D是有颜色的气体 |
| B.若升高温度,C的百分含量减少,则说明正反应为放热反应 |
| C.若增大压强,平衡不移动,则说明B和D一定都是气体 |
| D.如果B是气体,则增大A的浓度会使B的转化率增大,A的转化率减少 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 eC(g)+fD(g)在反应过程中,当其他条件不变时,C的体积分数
eC(g)+fD(g)在反应过程中,当其他条件不变时,C的体积分数 (C)在不同温度(T)和不同压强(P)的条件下随时间(t)的变化关系如图所示。下列叙述正确的是 ( )
(C)在不同温度(T)和不同压强(P)的条件下随时间(t)的变化关系如图所示。下列叙述正确的是 ( )
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
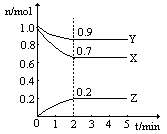
| A.该反应已停止 |
| B.单位时间内氮气的消耗速率等于氢气的生成速率 |
| C.3v(H2)=2v(NH3) |
| D.c(H2) :c(N2) :c(NH3) =" 7" :9 :2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com