
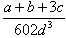 (3分)
(3分)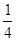 =3个、8×
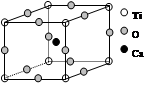
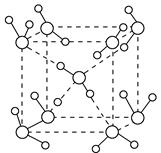
=3个、8×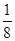 =1个、1个,即晶体结构中,元素氧、钛、钙的离子个数比是3:1:1,所以该物质的化学式可表示为CaTiO3。
=1个、1个,即晶体结构中,元素氧、钛、钙的离子个数比是3:1:1,所以该物质的化学式可表示为CaTiO3。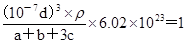 ,解得密度ρ=
,解得密度ρ=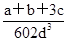 g/cm3。
g/cm3。

科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属具有良好的导电性,是因为金属晶体中的“电子气”在电场作用下作定向移动 |
| B.金属具有良好的导热性能,是因为自由电子受热后运动速率增大,与金属离子碰撞频率增大,传递了能量 |
| C.金属晶体具有良好的延展性,是因为金属晶体中的原子层在滑动过程中金属键未破坏 |
| D.金属一般具有银白色光泽,是物理性质,与金属键没有关系 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

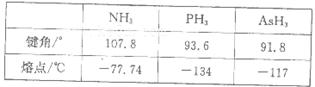
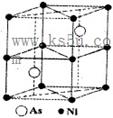
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
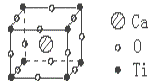
| A.CaTiO3 | B.CaTiO6 | C.Ca4TiO3 | D.CaTiO12 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.C70的熔点比石墨的熔点低 |
| B.C70和金刚石是同素异形体 |
| C.C70分子中含有70个σ键,35个π键 |
| D.C70Cl10分子中共用电子对数目为145个 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
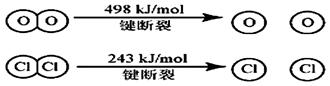
| 晶体 | NaCl | KCl | CaO |
| 晶格能/(kJ·mol-1) | 786 | 715 | 3401 |
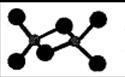
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
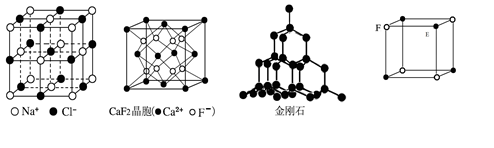
| A.在NaCl晶体中,距Na+最近的Cl-形成正八面体 |
| B.在CaF2晶体中,每个晶胞平均占有4个Ca2+ |
| C.在金刚石晶体中,碳原子与碳碳键数目比为1:2 |
| D.该气态团簇分子的分子式为EF或FE |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com