
| A�� | �����Ҵ������Ȼ�̼������Ҫ�л��ܼ�������������ȡ��ˮ�еĵⵥ�� | |
| B�� | ��ǿ������Һ�У�[Al��OH��4]-��HCO3-��Na+��Ca2+����ͬʱ�������� | |
| C�� | ��������Ƕп�飬����ԭ��أ�п���������Է����屻��ʴ | |
| D�� | ����Ͳ��ȡ10��mL 1.0mol/L��������100mL��Һƿ�У���ˮϡ�����̶ȣ����Ƶ�0.1mol/L������ |
���� A����ȡ��ˮ�еĵ���Ҫ������ȡ�����������õⵥ���ڻ����ܽ�������ܼ��е��ܽ��Բ�ͬ��Һ���룻
B��ǿ����Һ��̼��������ֲ��ܴ��ڣ�
C����п�ڵ������Һ���γ�ԭ��أ����ý���п����������ʴ����������������
D������������ƿ��ֱ���ܽ�������Һ��
��� �⣺A���Ҵ����ˮ���ܲ��ֲܷ㣬������ȡ�ⵥ�ʣ���A����
B��ǿ����Һ��HCO3-+OH-=H2O+CO32-������̼��������Ӳ��ܴ������ڣ���B����
C����������Ƕп�飬����ԭ��أ����ý���п����������ʴ���������������������屻��ʴ���ã���C��ȷ��
D������Ͳ��ȡ10.0 mL1.00 mol•L-1���ᣨ��ȡ���������ᵹ���ձ��У�������ˮϡ�ͣ��ܽ�ϡ�ͣ���ת�Ƶ�100ml ����ƿ�У�ת�ƣ���ϴ�Ӳ��������ձ���һ����������ƿ�У�ϴ�ӣ�����ˮ���̶��ߣ����ݣ���ת�Ƶ��Լ�ƿ����D����
��ѡC��
���� ���⿼���˻�����ᴿ���������ӹ�����жϡ�ԭ���ԭ����Ӧ�á�������Һ�IJ������յȣ���Ŀ�ϼ������ڿ���ѧ���Ի���֪ʶ���ۺ�Ӧ��������ע�������Һ�����Ʒ�����


 ��ҵ����ϵ�д�
��ҵ����ϵ�д� ͬ��ѧ��һ�ζ���ϵ�д�
ͬ��ѧ��һ�ζ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
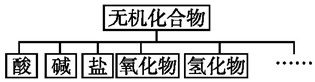
| ������� | �� | �� | �� | ������ | �⻯�� |
| ��ѧʽ | ��HCl ��H2SO4 | ��NaOH ��Ba��OH��2 | ��Na2CO3 ��K2SO4 | ��CO2 ��Na2O | ��NH3 ��H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
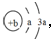 ��Y��ZΪͬ���ڽ���Ԫ�أ�����YΪ������Ԫ����ԭ�Ӱ뾶����Ԫ�أ�ZΪ�ؿ��к�����ߵĽ���Ԫ�أ�W������������Ӧˮ�������������̬�⻯�ﷴӦ������G����G��Һ�����ԣ��ش��������⣺
��Y��ZΪͬ���ڽ���Ԫ�أ�����YΪ������Ԫ����ԭ�Ӱ뾶����Ԫ�أ�ZΪ�ؿ��к�����ߵĽ���Ԫ�أ�W������������Ӧˮ�������������̬�⻯�ﷴӦ������G����G��Һ�����ԣ��ش��������⣺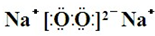 �������еĻ�ѧ������Ϊ���Ӽ����ۼ���
�������еĻ�ѧ������Ϊ���Ӽ����ۼ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ũ���ᡢŨ�����Ũ���᳤�ڱ�¶�ڿ����У����������С��Ũ�ȶ��ή�� | |
| B�� | ��ˮ�ͻ���̿����ʹ��īˮ��ɫ����ԭ����ͬ | |
| C�� | Ũ��������ֽ⣬����ʱ��ʵ���ҿ�����Ũ����ʻ�ɫ | |
| D�� | ŨH2SO4��ǿ�����ԣ�����������Cu�������ҷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe2+ NO3- I-SO42- | B�� | MnO4- K+NO3-Na+ | ||
| C�� | K+Al3+Cl-SO42- | D�� | Mg2+SO32-Br-Ba2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������Դ���滯ʯȼ�ϣ������ڽ�Լ��Դ���������� | |
| B�� | ʳƷ���Ӽ�����ܶ࣬���е�һ��Ϊ�������ƣ����DZ���һ��ͬϵ������Ӧ������ | |
| C�� | ����ҩ������ܶ࣬��̼�����ơ�̼��ơ�̼��þ������������������þ�� | |
| D�� | ijЩ�߲˺�ˮ���������л�����ɼ������ʣ����Գ�Ϊ����ʳ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ij��Ԫ�������ʽ��NaHA��Һ�У�c��H+��+c��Na+��=c��OH-��+c��HA-��+c��A2-�� | |
| B�� | ���ʵ���Ũ����ȵĢ�NH4HCO3��Һ����NH4Cl��Һ����NH4HSO4��Һ�У�c��NH4+���Ĵ�С��ϵ���٣��ڣ��� | |
| C�� | 0.1 mol•L-1 CH3COONa ��Һ��0.05 mol•L-1����������Ϻ��������Һ�У�c��CH3COO-����c��Cl-����c��CH3COOH����c��H+�� | |
| D�� | 0.1mol•L-1��NH4��2Fe��SO4��2��Һ�У�c��NH4+��+c��NH3•H2O��+c��Fe2+��=0.3 mol•L-1 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com