
| | 操作 | 现象 | 结论 |
| A | 向某无色溶液中滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| B | 向某溶液中先滴加KSCN溶液,再滴加少量氯水 | 先无明显现象,后溶液变成血红色 | 原溶液中含有Fe2+和Fe3+ |
| C | 将铜片放入浓硝酸中 | 产生大量红棕色气体,溶液变为蓝绿色 | 浓硝酸有强氧化性和酸性 |
| D | 向Na2SiO3溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去 | 2 min后,试管里出现凝胶 | 酸性:硅酸>盐酸 |
科目:高中化学 来源:不详 题型:单选题
| A.除去Mg粉中的Al粉:加入足量NaOH溶液后,过滤、洗涤 |
| B.除去BaCO3固体中混有的BaSO4:加入过量盐酸后,过滤、洗涤 |
| C.除去CO中混有的CO2:用足量NaOH洗气 |
| D.除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.稀H2SO4 | B.NaOH溶液 | C.BaCl2溶液 | D.Ba(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.向某溶液中加入Na2CO3溶液,若有白色沉淀生成,证明一定含有Ca2+ |
| B.向某固体中加入稀盐酸,产生了无色气体,证明该固体一定含有CO32— |
| C.向某溶液中滴加KSCN溶液,若溶液出现红色则说明原溶液中含Fe3+ |
| D.向某溶液中先加稀硝酸,再加BaC12溶液,生成白色沉淀,证明一定含有SO42— |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
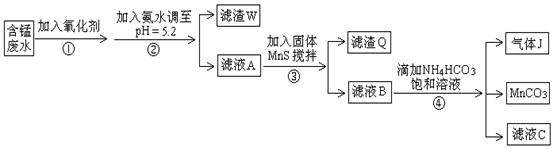
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 | Mn(OH)2 | CuS | MnS | MnCO3 |
| 沉淀完全时的PH | 3.7 | 5.2 | 6.4 | 9.8 | ≥0 | ≥7 | ≥7 |
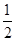 O2 → MnO2 + CO2。
O2 → MnO2 + CO2。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
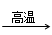 4CO(g) + BaS(s)工业上以重晶石矿(主要成分BaSO4,杂质为Fe2O3、SiO2)为原料,通过下列流程生产氯化钡晶体(BaCl2·nH2O)。
4CO(g) + BaS(s)工业上以重晶石矿(主要成分BaSO4,杂质为Fe2O3、SiO2)为原料,通过下列流程生产氯化钡晶体(BaCl2·nH2O)。
 4CO + CaS+ BaCl2。请你完善下列从焙烧后的固体中分离得到氯化钡晶体的实验流程的设计(已知硫化钙不溶于水,易溶于盐酸)。
4CO + CaS+ BaCl2。请你完善下列从焙烧后的固体中分离得到氯化钡晶体的实验流程的设计(已知硫化钙不溶于水,易溶于盐酸)。
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
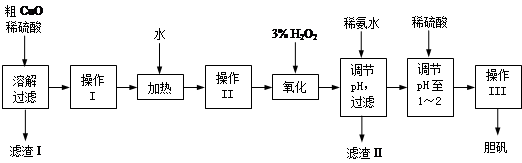
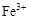 、
、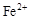 、
、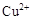 转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:| | 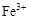 | 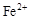 | 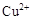 |
| 开始沉淀时的pH | 2.7 | 7.6 | 5.2 |
| 完全沉淀时的pH | 3.7 | 9.6 | 6.4 |
| | 第一次实验 | 第二次实验 |
| 坩埚质量(g) | 14.520 | 14.670 |
坩埚质量 晶体质量(g) 晶体质量(g) | 17.020 | 18.350 |
| 第一次加热、冷却、称量(g) | 16.070 | 16.989 |
| 第二次加热、冷却、称量(g) | 16.070 | 16.988 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 2NaVO3 +2NaAlO2 +2CO2
2NaVO3 +2NaAlO2 +2CO2
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.肯定有SO2、HCl | B.一定没有CO2、HBr、NO2 |
| C.可能有HBr、CO2 | D.一定有SO2,可能有HCl、CO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com